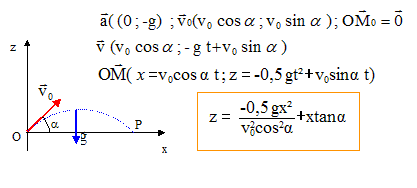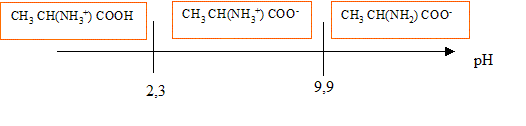|
Projectile; dipole LC, acide base, alanine, ammoniac, mťthylamine d'aprŤs concours
controleur de la concurence et de la rťpression des fraudes 2004 En
poursuivant votre navigation sur ce site, vous acceptez l’utilisation
de Cookies vous proposant des publicitťs adaptťes ŗ vos centres
d’intťrÍts.
|
|||||||||||||||||||||
| .
. |
|||||||||||||||||||||
|
|||||||||||||||||||||
|
|
Un homme ťtudie le mouvement d.un projectile de centre de gravitť G et de masse m, dans un champ uniforme de pesanteur terrestre. Le sol est horizontal. Les forces de frottements sont considťrťes comme nťgligeables ainsi que la poussťe d.ArchimŤde. Soit un repŤre du rťfťrentiel terrestre tel que l'origine O coÔncide avec la position du projectile ŗ l'instant t = 0 du lancement. L'axe vertical orientť vers le haut et le plan (x O z) contient le vecteur vitesse initiale V0 qui fait un angle a avec l'axe horizontal. 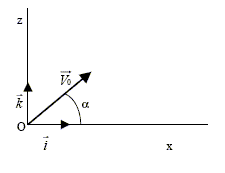
corrigť chute libre : la balle n'est soumise qu'ŗ son poids, vertical, vers le bas, valeur mg. Ecrire la seconde loi de Newton la vitesse est une primitive de l'accťlťration ; la position est une primitive de la vitesse.
y=0 : le mouvement s'effectue dans le plan vertical dťfini par les vecteurs accťlťration et vitesse initiale. Sur l'axe Ox, la composante du vecteur vitesse est constante, ťgale ŗ v0 cos a : le mouvement est uniforme sur l'axe Ox horizontal. En retombant sur le sol z = 0 soit : -0,5 g x≤ / (v0≤cos≤a) + x sin a /cos a =0 multiplier par cos a et diviser par x : -0,5 g x / (v0≤cosa) + sin a =0 0,5 gx = v0≤cosa sin a ; x = 2 v0≤cosa sin a / g = v0≤ sin (2a) / g cette distance est maximale si sin (2a) = 1 soit a = 45į.
|
||||||||||||||||||||
|
Un condensateur de capacitť C= 20 mF chargť sous une tension U= 5 V est branchť aux bornes d'une bobine d'inductance L = 50 mH.
corrigť 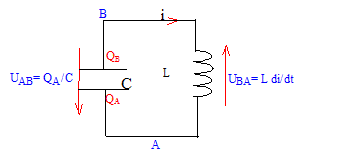
L'armature QA porte une charge nťgative ; QB= -QA. uc = UAB Les oscillations sont-elles libres ; aucun gťnťrateur n'est prťsent : ce dernier forcerait le circuit (LC)ŗ osciller ŗ la frťquence du gťnťrateur. UAB + UBA=0 ; QA/C + Ldi/dt = 0 ; i = dQA/dt ; di/dt =d≤QA/dt≤ d'oý : QA/C + Ld≤QA/dt≤ = 0 soit : d≤QA/dt≤ +QA/ (LC ) = 0 La pulsation propre w0 s'exprime en radian/seconde ; sa valeur est telle que w02 = 1/(LC) = 1/( 0,05*2 10-5) = 106. w0 = racine carrťe (106) = 103 rad/s. pťriode propre : T0 = 2p /w0 =6,28 / 103 =6,28 10-3 s. uc = U cos(w0 t ); QA = C UAB = C U cos(w0 t) dťriver deux fois par rapport au temps : dQA /dt = -w0C U sin(w0 t) ; d≤QA /dt≤ = -w≤0C U cos(w0 t) ; repport dans l'ťquation diffťrentielle : d≤QA/dt≤ +QA/ (LC ) = 0 avec w02 = 1/(LC) -w≤0C U cos(w0 t) + C U/ (LC) cos(w0 t) = 0 est vťrifiťe quelle que soit le temps Donc uc = U cos(w0 t ) reprťsente la tension aux bornes du condensateur ŗ t=0 le condensateur est chargť et la tension ŗ ces bornes vaut : Umax = 5 V d'oý uc = 5 cos(w0 t ) L'ťnergie initiale du dipole (LC) est stockťe par le condensateur et vaut : E=ĹCU≤ = 0,5*20 10-6 *25 = 6,25 10-4 J Au cours du temps il y a ťchange d'ťnergie entre condensateur et bobine inductive. E= ĹLi≤(t) + ĹCu≤c(t) Si la rťsistance du circuit est nulle, l'ťnergie se conserve. |
|||||||||||||||||||||
|
Donnťes : N( Z=7) ; H (Z=1) ; masse atomique mlolaire (g/mol) : N : 14 ; H : 1. constante d'aciditť : NH4+/NH3 : pKa = 9,2 ; CH3NH3+ / CH3NH2 : pKa = 10,75 ; alanine : pKa1 = 2,3 et pKa2 = 9,9.
corrigť configuration ťlectronique de l’atome d’hydrogŤne : K1 de l’atome d’azote : K2L5. nature des liaisons dans la molťcule d’ammoniac : covalente polarisťe, l'atome d'azote attire ŗ lui le doublet de liaison. gťomťtrie de cette molťcule : pyramide ŗ base triangulaire, l'atome dazote est au sommet de la pyramide et porte un doublet non liant ( type AX3 Ed ans la mťthode VSEPR) angle HNH : 107 į, infťrieur ŗ 109į car le doublet non liant repousse les trois doublets liants.
ťquation bilan de la rťaction de dosage : NH3 + H3O+ = NH4+ + H2O ŗ l'ťquivalence du dosage, les quantitťs de matiŤre des rťactifs sont en proportions stoťchiomťtriques : n(NH3) = 100 C ; n(H3O+) = 1,1*8 = 8,8 C= 8,8 / 100 = 8,80 10-2 mol/L nature de la solution ŗ l’ťquivalence : chlorure d'ammonium NH4+ ; Cl-. le pH ŗ l’ťquivalence : [H3O+]≤= Ka C ; 2 log [H3O+] = log Ka + log C ; pH = Ĺ(pKa-log C) pH= 0,5 (9,2-log (8,80 10-2 ) = 5,1. le pH ŗ l'ťquivalence doit appartenir ŗ la zone de virage de l'indicateur colorť : rouge de mťthyle concentration de la solution commerciale de densitť 0,88 et dont le pourcentage en masse d’ammoniac est de 32 % : masse de 1 L de solution : 880 g ; masse d'ammoniac pure : 880*0,32 =281,6 g masse molaire ammoniac : 14+3 = 17 g/mol concentration : 281,6 / 17 = 16,5 mol/L.
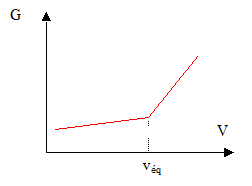
avant l'ťquivalence, dans l'erlenmeyer , l'acide est en dťfaut : les molťcules d'ammoniac rťagissent avec les ions oxonium ajoutťs ; on ajoute des ions chlorure et il se forme des ions ammonium. Seuls les ions contribuent ŗ la conductivitť de la solution : tout se passe, du point de vue de la conductivitť comme si on remplaÁait des molťcules NH3 par des ions NH4+ et Cl-. La conductivitť de ces ions n'est pas trŤs grande ( comparťe ŗ celle de l'ion oxonium) : la conductivitť de la solution augmente lentement. Conductance et conductivitť ťtant proportionnelles, la conductance augmente lentement. aprŤs l'ťquivalence, dans l'erlenmeyer , l'acide est en excŤs : on ajoute des ions H3O+ et Cl-. La conductivitť de l'ion oxonium ťtant 5 fois plus grande que celle des ions Cl- et NH4+, la conductivitť, donc la conductance augmente fortement.
|
|||||||||||||||||||||
|
On considŤre les deux composťs, ammoniac et mťthylamine.
corrigť formule semi dťveloppťe de la molťcule de mťthylamine : CH3-NH2 amine primaire NH3 + H2O = NH4++HO-avec [NH4+]= [HO-] = 10-14/[H3O+] = 10-14/10-11,1 = 10-2,9 CH3-NH2 + H2O = CH3NH3+ + HO- avec [CH3NH3+]= [HO-] = 10-14/[H3O+] = 10-14/10-11,9 = 10-2,1 Ces molťcules sont des bases : on observe l'apparition d'ion hydroxyde en solution. taux de protonation a = [NH4+] / C = 10-2,9/0,1 = 10-1,9 = 1,25 10-2 ( 1,25 %) a = [CH3NH3+] / C = 10-2,1/0,1 = 10-1,1 = 8 10-2 ( 8 %) Comparer la force du caractŤre acidobasique de ces deux composťs : le taux de protonation est plus grand pour la mťthylamine : celle ci est une base plus forte que l'ammoniac ŗ concentration ťgale.
|
|||||||||||||||||||||
|
L’alanine a pour formule chimique CH3 CH(NH2) COOH. Ce composť existe ŗ l’ťtat solide et en solution aqueuse sous la forme d’un amphion ou ion dipolaire ou zwittťrion de formule chimique CH3 CH(NH3+) COO-.
corrigť Dans la molťcule d'alanine on trouve deux fonctions chimiques : une fonction amine -NH2 au caractŤre basique et une fonction acide carboxylique, au caractŤre acide. Base conjuguťe de l’amphion : CH3 CH(NH2) COO- ; acide conjuguť de l’amphion : CH3 CH(NH3+) COOH Les couples acide base sont : CH3 CH(NH3+) COOH / CH3 CH(NH3+) COO- pKa1 = 2,3 CH3 CH(NH3+) COO- / CH3 CH(NH2) COO- pKa2 = 9,9.
Lorsqu'on dissout de l'alanine dans l'eau, elle est essentiellement sous forme d'ion dipolaire -OOC-RCH-NH3+,( du fait de la forte solubilitť dans l'eau) la concentration en molťcules HOOC-RCH-NH2 est nťgligeable. HOOC-RCH-NH3+
+ H2O = -OOC-RCH-NH3+
+ H3O+ pKa1=
2,3 AH+ + H2O = A+ H3O+ ; Ka1 = [A] h / [AH+] = 10-2,3 = 0,005. A + H2O = A- + H3O+ ; Ka2 = [A-]h / [A]= 10-9,9 = 1,25 10-10 conservation A : [AH+]+[A]+[A-]=0,1 ; or A majoritaire dans l'eau : [A] voisin 0,1 mol/L solution ťlectriquement neutre : h+ [AH+] = [OH-]+[A-] hypothŤse : h et [OH-] nťgligeable devant [AH+] et [A-] alors [AH+] =[A-] Ka1 * Ka2 = h≤[A-] / [AH+] = 6,25 10-13 h≤= 6,25 10-13 ; pH= 6,1. si on calcule [AH+] et [A-] on trouve : [AH+] = [A] h/Ka1 = 0,1 * 10-6,1 / 0,005 = 1,6 10-5 alors que h= 7,8 10-7 [A-] =Ka2[A]/h= 1,25 10-10*0,1/ 10-6,1 = 1,6 10-5 ; hypothŤse confirmťe
|
|||||||||||||||||||||
|
|