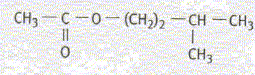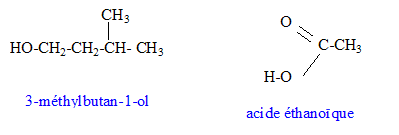|
En poursuivant votre navigation sur ce site, vous acceptez l’utilisation de Cookies vous proposant des publicitťs adaptťes ŗ vos centres d’intťrÍts. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| .
. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
On donne l'ťquation de rťaction suivante,ainsi que la constante d'ťquilibre associťe : Cu(s) + Zn2+(aq) = Zn(s) + Cu2+(aq) ; K= 5,0 10-38.
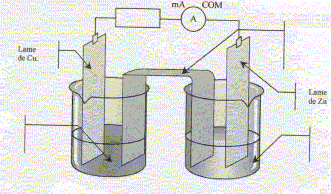
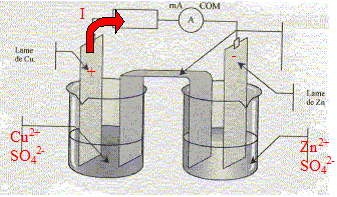
corrigť Sens d'ťvolution du systŤme chimique : On trempe une lame de zinc et une lame de cuivre dans un becher contenant V1= 100 mL d'une solution de sulfate de cuivre (Cu2+ + SO42-), de concentration en ion Cu2+ donnťe par [Cu2+]i = 0,5 mol/L et un volume V2= 100 mL d'une solution de sulfate de zinc (Zn2+ + SO42-) de concentration en ion Zn2+ donnťe par [Zn2+]i = 0,5 mol/L. Inventaire des espŤces chimiques prťsentes ŗ l'ťtat initial : H2O,
Cu(s), Zn(s), Zn2+ , SO42-,
Cu2+ Qr i
= [Cu2+]i / [Zn2+]i
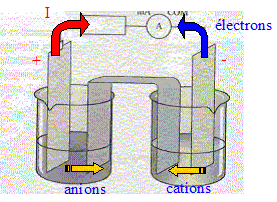
=1, valeur supťrieure ŗ K. Les branchements ŗ rťaliser pour mesurer une tension positive aux bornes de la pile : voltmŤtre en dťrivation, borne COM sur le zinc ; borne "V" sur le cuivre Les porteurs de charges dans les ťlectrolytes : les ions positifs ou cations : ils se dťplacent dans le sens du courant. les ions nťgatifs ou anions : ils se dťplacent en sens contraire du courant. et dans les mťtaux : les ťlectrons ; ils se dťplacent en sens contraire du courant
Les demi-ťquations ťlectroniques mises en jeu aux ťlectrodes : anode nťgative, oxydation du zinc : Zn(s) = Zn2+ + 2e-. cathode positive (
Cu), rťduction de Cu2+ : Cu2+
+2e- = Cu(s) Les rťsultats trouvťs sont en accord avec le critŤre d'ťvolution.
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
L'arŰme de banane est obtenu en synthťtisant
un composť organique : l'acťtate d'isoamyle
corrigť Le groupe caractťristique contenu dans l'acťtate d'isoamyle : 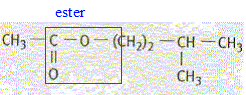
L'acťtate d'isoamyle est obtenu ŗ partir de l'acide ťthanoÔque et du 3-mťthylbutan-1-ol. Les formules semi-dťveloppťes de ces composťs sont :
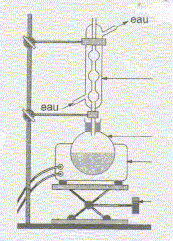
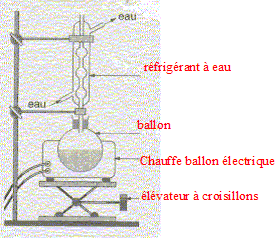
Equation chimique relative ŗ la transformation chimique prťcťdente : CH3-COOH + HO-CH2-CH2-CH(CH3)2 = CH3-COO-CH2-CH2-CH(CH3)2 +H2O Le signe = traduit le fait que l'on aboutit ŗ un ťquilibre chimique. Ces caractťristiques cinťtiques : lente, athermique, limitťe par l'hydrolyse de l'ester. Chauffage ŗ reflux :
Le taux d'avancement final est de 67 %. Taux d'avancement final d'une rťaction : t = xfin
/ xmax avec x l'avancement (mol)
Masse d'acťtate d'isoamyle obtenue(g) = Quantitť de matiŤre (mol) * masse molaire (g/mol) m= 0,67*150 = 2/3*150 = 100 g. Pour amťliorer ce taux on modifie certaines conditions expťrimentales :
expťrience 2 : l'acide sulfurique est un catalyseur ; l'ťquilibre est plus rapidement atteint ( par rapport ŗ l'expťrience 0) mais la composition du mťlange ŗ l'ťquilibre n'est pas modifiťe ( t inchangť) expťrience 3 : l'acide sulfurique est un catalyseur ; la quantitť de matiŤre des rťactifs est un facteur cinťtique ; l'ťquilibre est plus rapidement atteint ( par rapport ŗ l'expťrience 0) et la composition du mťlange ŗ l'ťquilibre est modifiťe ; en ajoutant l'alcool en excŤs, l'ťquilibre est dťplacť vers la droite, formation de l'ester ( t augmente) On peut rťaliser la synthŤse en remplaÁant l'acide par un autre composť organique. 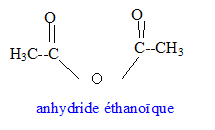 Equation bilan associťe ŗ la transformation chimique : [CH3-CO]2O
+ HO-CH2-CH2-CH(CH3)2
--> CH3-COO-CH2-CH2-CH(CH3)2
+CH3-COOH
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|