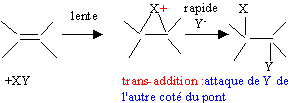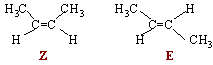|
En poursuivant votre navigation sur ce site, vous acceptez l’utilisation de Cookies vous proposant des publicitťs adaptťes ŗ vos centres d’intťrÍts. |
||
| .
. |
||
|
||
|
|
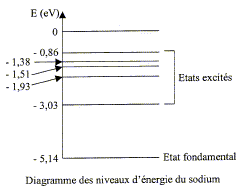
Le numťro atomique de l'ťlťment sodium est Z=11. L'analyse du spectre d'ťmission d'une lampe ŗ vapeur de sodium rťvŤle la prťsence de raies de longueurs d'onde bien dťfinies : 
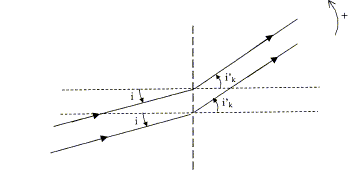
On rappelle la formule d'un rťseau ŗ n traits mm-1 : sin ik' -sin i = kln, dťfinissant pour une incidence i les directions ik' dans lesquelles se trouvent les maximas de lumiŤre d'une radiation monochromatique de longueur d'onde l.
corrigť structure ťlectronique de l'ťlťment sodium : 11 ťlectrons dans l'ťtat fondamental :1s2 2s2 2p6 3s1. domaine de longueurs d'ondeauquel appartiennent ces radiations : l1 < 400 nm donc domaine U V. l2 , l3 , l'3, l4 : domaine visible l5 , l6, valeurs supťrieures ŗ 800 nm : domaine I R. Calcul de la frťquence de la radiation jaune de longueur d'onde l3=589,0 nm = 5,89 10-7 m n = c/l3 =3 108 / 5,89 10-7 = 5,09 1014 Hz. Calcul de l'ťnergie ( en J et en eV) des photons correspondants : E= hc/l3 = 6,63 10-34*3 108 / 5,89 10-7 =3,38 10-19 J ; diviser par 1,6 10-19 : 2,11 eV. En utilisant le diagramme simplifiť des niveaux d'ťnergie de l'atome de sodium, on trouve que l'ťcart ťnergťtique entre le niveau excitť n=1 et le fondamental vaut : -3,04+5,14 = 2,11 eV ; cette radiation jaune correspond donc ŗ la transition de l'ťtat excitť 1 vers l'ťtat fondamental. Un atome de sodium ŗ l'ťtat fondamental ne peut pas absorber un photon d'ťnergie 3 eV : l'ťnergie du photon doit Ítre ťgale ŗ la diffťrence d'ťnergie entre un ťtat excitť et l'ťtat fondamental.
La formule des rťseaux traduit le fait que dans la direction dťfinie par sin ik' pour un angle i donnť, les ondes diffractťes par toutes les fentes sont en phase. n: nombre de traits par unitť de longueur a=1 / n pas du rťseau k appartient ŗ Z k est appelť l'ordre l longueur
d'onde (m) de la lumiŤre utilisťe.
Calcul des angles ik' des directions dans lesquelles on a des maxima de lumiŤre pour une radiation de longueur d'onde l = 589 nm. n = 750 traits / mm. le nombre de maxima principaux est fini : pour i =0 ; n =7,5 105 traits m-1 ; l=589 10-9 m sin ik' = kln soit sin ik' = 7,5 105 *589 10-9 k= 4,417 10-1 k k=0 donne i0' =0 ; k =1 donne i1'
= + ou - 26,21į; k =2 donne i2' = + ou - 62,06į.
Calcul de l'ťcart angulaire D ik' entre les directions ik' des maxima des radiations ŗ l3 = 589 nm et l'3 =589,6 nm du spectre du sodium. sin ik' = 7,5 105 *589,6 10-9
k= 4,422 10-1 k - ŗ l'ordre k=2 : i2'
= + ou - 62,18į; D
ik' = 0,12 į
A l'ordre k=1, le pouvoir sťparateur vaut : R= N= 7,5 105*0,02 = 1,5 104 traits utilisťs ; l/Dlm = 589 10-9 / 0,6 10-9
= 982 ; R > l/Dlm
|
|
|
pKa du couple (NH4+ / NH3) = 9,20 ŗ 25įC ; 11H ; 147N. L'ammoniac est un gaz molťculaire de formule NH3 trŤs soluble dans l'eau.
corrigť Structure : modŤle de Lewis de la molťcule d'ammoniac. 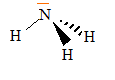 gťomťtrie de la molťcule d'aprŤs la thťorie VSEPR : type AX3E donc pyramide ŗ base triangulaire pH d'une solution : L'ammoniac est donc une base selon Lewis.. couples acide base mis en prťsence : NH4+ / NH3 et H2O / HO-. NH3 + H2O = NH4+ + HO-. On souhaite prťparer une solution tampon ŗ partir de
l'ammoniac. modŤre la variation du pH, faisant suite ŗ l'ajout
modťrť d'acide ou de base forte. Les concentrations de la base NH3
et de son acide conjuguť NH4+
sont ťgales : en consťquence pH=pKa = 9,2.
|
||
|
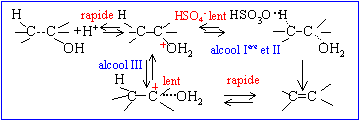
On souhaite, en deux ťtapes passer du but-1-Ťne au but-2-Ťne. Dans un premier temps le but-1-Ťne est hydratť ŗ froid en milieu acide sulfurique diluť. On obtient majoritairement un produit A.
corrigť ťquation bilan conduisant ŗ A : CH3-CH2-CH=CH2 + H2O = CH3-CH2-CHOH-CH3 : butan-2-ol mťcanisme rťactionnel de la rťaction en justifiant la formation majoritaire de A:
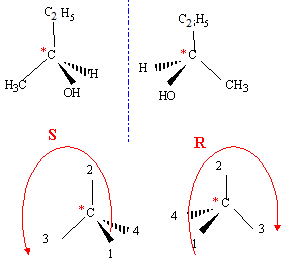
La rŤgle de Markovnikov permet de prťvoir sur quel atome de carbone se fixe l'hydrogŤne de l'hydracide ( ou de H2O) : l'atome d'hydrogŤne se fixe sur l'atome de carbone le moins substituť. Le produit A possŤde des stťrťoisomŤres ; reprťsentation de Cram et nomenclature RS.
Le composť A est maintenant dťshydratť en milieu acide sulfurique concentrť ŗ 150 įC. ťquation bilan de la rťaction prťcťdente : CH3-CH2-CHOH-CH3
= CH3-CH=CH-CH3 + H2O Dans le cas ou plusieurs atomes de carbone sont porteurs d'hydrogŤnes pouvant Ítre ťliminťs, l'alcŤne le plus substituť se forme.
Le but-2-Ťne prťsente une stťrťoisomťrie de type Z E :
|
||
|
|