1.1. Calculer le
volume maximal V
max܄ d’eau de pluie récupérable par an pour un toit
ondulé en pente bien
entretenu de surface S
toit = 50 m
2 à Auxerre.
V
max = p S
toit K
T K
f.
p = 0,700 m précipitations annuelles.
K
T = 0,80 coefficient de restitution.
K
F = 0,90 coefficient de rendement hydraulique.
V
max = 0,700 x 50 x0,80 x 0,90 =25,2 m
3.
1.2. Calculer combien de fois la cuve pourra être remplie par an.
Données
Hauteur de la cuve : H = 1,00 m.
Surface de la base de la cuve : S
cuve = 5,00 m
2.
Volume de la cuve : H S
cuve = 5,00 m
3.
La cuve pourra être remplie 5 fois par an.
Pour vérifier le volume d’eau contenu dans la cuve de récupération, celle-ci est équipée d’un capteur.
1.3. Indiquer si les ondes utilisées par le capteur sont des ondes
électromagnétiques ou des ondes mécaniques. Justifier la réponse.
1.4. Indiquer à quel domaine ces ondes appartiennent.
La sonde utilise des ondes ultrasonores de fréquence 40 kHz. Ce sont des ondes mécaniques.
La sonde permet d’obtenir des mesures de hauteur. Les oscillogrammes présentés ci-dessous en sont une
illustration.
1.5. Associer à chaque situation A et B présentée ci-dessous l’oscillogramme 1 ou 2 qui lui correspond.
Expliquer votre démarche.
 Situation A
Situation A : la distance entre le capteur et l'eau est faible. La durée séparant l'émission et la réception sera courte. Oscillogramme 2.
Situation B
: la distance entre le capteur et l'eau est 2 fois plus grande qu'en A.
La durée séparant l'émission et la réception sera 2 fois plus grande.
Oscillogramme 1.
1.6. Déterminer la durée
Dt entre l’émission et la réception du signal pour la cuve
étudiée (oscillogramme 2.).
4 divisions soit 4,00 ms.
1.7. Vérifier alors que la hauteur h mesurée entre le capteur et la surface de l’eau
vaut 68,0 cm.
2 h = c
Dt avec c = 340 m /s.
h = 340 x 4,0 10
-3 / 2 =0,68 m.
Un point de pompage, dans la cuve, permet d’envoyer l’eau de pluie récupérée dans les installations
sanitaires. Ce point de pompage est situé à une hauteur h’ = 25,0 cm du fond de la cuve.
1.8. Vérifier alors si le niveau de l’eau de pluie récupérée est suffisant pour le système de pompage.
Hauteur d'eau dans la cuve : 1,0-0,68 = 0,32 m, valeur supérieure à h' = 0,25 m.
Une autre sonde est testée en laboratoire dans des conditions expérimentales similaires à l’utilisation de la
sonde commerciale dans la cuve.
1.9. Justifier la relation de la ligne 17 du programme du microcontrôleur.
h = v * t / 2 / 10000.
h : distance en cm entre l'objet et la sonde.
v = 340 m /s, vitesse du son dans l'air.
t durée entre l'émission et la réception en microseconde.
h x 10
-2= v t x10
-6 / 2 ; h = v t 10
-4 / 2 = v t /2 / 10000.
.
Les résultats des mesures de la hauteur h par la sonde HC-SR04 sont présentées dans le tableau cidessous :
mesure
|
1
|
2
|
3
|
4
|
5
|
6
|
7
|
8
|
9
|
10
|
11
|
12
|
13
|
14
|
15
|
h(cm)
|
68;0
|
65,5
|
68,0
|
68,0
|
67,9
|
67,9
|
68,0
|
68,0
|
68,0
|
67,9
|
67,8
|
68,0
|
67,9
|
67,9
|
68,0
|
1.10. Calculer l’incertitude-type u(h) sur la mesure de la hauteur h avec un écart type expérimental de
0,64 cm.
u(h) = 0,64 / 15
½ =0,165 ~0,17 cm.
1.11. Proposer au minimum 2 avantages et 2 inconvénients de chaque sonde dans le cadre d’une utilisation
dans une cuve de récupération.
Avantages : plage de mesures importante, jusu'à 15 m.
Robustesse, bonne étanchéité, connectivité Bluetooth.
Inconvénients : prix élevé 1000 €. Durée de vie inconnue.
Acidité de l'eau de pluie.
Parmi les différentes espèces chimiques intervenant dans l’acidité de l’eau de pluie, on ne s’intéresse dans
la suite qu’au dioxyde de carbone.
Deux couples acides/bases sont alors mis en jeu : CO
2, H
2O aq / HCO
3-aq et
HCO3-aq / CO32-aq.
A.1. Citer un moyen d’estimer le pH d’une solution.
Utiliser un papier indicateur universel de pH.
A.2. Justifier que le dioxyde de carbone dissout
CO2, H2O aq est un acide au sens de Brönsted.
CO2, H2O aq est susceptible de réagir avec l'eau en donnant H3O+aq , c'est donc un acide an sens de Brönsted.
A.3. Établir le diagramme de prédominance mettant en jeu les deux couples acide/base.
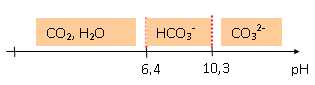 A.4.
A.4. La valeur du pH de l’eau de pluie récupérée dans la cuve est de 4,8 à 25° C. Déterminer alors l’espèce
chimique prédominante dans cette eau de pluie.
A pH inférieur à 6,4,
CO2, H2O aq prédomine.
A.5. Établir l’équation de la réaction du dioxyde de carbone dissout avec l’eau.
CO2, H2O aq + H2O(l) = HCO3-aq + H3O+aq.
A.6. En déduire l’expression littérale de la constante d’acidité K
a liée à la réaction du dioxyde de carbone
dissout avec l’eau.
K
a = [
HCO3-aq] [
H3O+aq] / [
CO2, H2O aq].
D’après un rapport d’office parlementaire du sénat sur la qualité de l’eau, une eau de pluie est considérée
comme très acide dans le cas où
[HCO3-aq] / [CO2, H2O aq] < 0,040.
A.7. Calculer le quotient
[HCO3-aq] / [CO2, H2O aq]
pour l’eau de pluie récupérée et conclure sur son caractère très acide.
[HCO3-aq] / [CO2, H2O aq] = Ka / [H3O+aq] =10-6,4 / 10-4,8 =10-1;6 ~ 0,025.
0,025 < 0,040, l'eau est considérée comme très acide.