Boissons
énergisantes ou énergétiques,
bac S Antilles septembre 2019.
En
poursuivant votre navigation sur ce site, vous acceptez l’utilisation
de Cookies vous proposant des publicités adaptées à vos centres
d’intérêts.
| .
. |
Composition partielle de 100 mL de boisson :
|
Boisson énergisante A
|
Boisson énergétique B
|
Boisson énergétique C
|
Caféine
|
32 mg
|
|
|
Taurine
|
400 mg
|
|
|
Glucuronolactone
|
240 mg
|
|
|
Sucre
|
10,8 mg
|
4,1 mg
|
5,7 mg
|
Vitamines
|
B6 : 5 mg
B2 : 1,5 mg
B12 :0,005 mg
|
|
C : 5,3 mg
B1 : 0,1 mg
|
Acide a aminés
|
|
|
Valine : 75 mg
Leucine : 150 mg
Isoleucine : 75 mg
|
Sels minéraux
|
|
Oui
|
Oui
|
M(taurine) =125 g / mol ; M(glucose) = 180 g/mol.
DJA(taurine) = 3 mg kg-1 jour-1 ; DJA(caféine) = 5 mg kg-1 jour-1 ; DJA(Glucuronolactone) = 17 à 34 mg kg-1 jour-1 ;
1. Dangers de la surconsommation de boissons énergisantes.
1.1.
Quelle(s) différence(s) d'un point de vue de la composition chimique,
existe-t-il entre boisson énergisante et boisson énergétique ?
Une boisson énergisante contient de la caféine,de la taurine, du
glucuronolactone et beaucoup de sucre. Les boissons énergétiques ne
contiennent pas ces espèces et contienent moins de sucres.
1.2. Quel volume
de boisson énergisante A un jeune adulte peut-il consommer par jour
sans que les espèces chimiques contenues dans cette boisson ne
présentent un risque pour la santé ?
Masse de la personne : 50 kg ;
DJA(taurine) = 3 mg kg-1 jour-1 soit 3 x50 = 150 mg / jour.
Volume maximum : 150 / 400 x 100=37,5 mL / jour.
DJA(caféine) = 5 mg kg-1 jour-1 soit 5 x50 = 250 mg / jour.
Volume maximum : 250 / 32 x100 ~780 mg / jour.
DJA(Glucuronolactone) = 17 à 34 mg kg-1 jour-1 soit entre 17 x50 =850 mg / jour et 34 x50 =1700 mg / jour
Volume maximum : 240 / 1700 x100 ~140 mL / jour.
Cet adulte peut consommer au maximum 37,5 mL de boisson A par jour.
Au dela de cette consommation, des symptômes cardiovasculaires,
psychocomportementaux, neurologiques et gastro-intestinaux peuvent
survenir. Il faut donc surveiller la commercialisation de ces boissons.
|
|
2. La caféine et la taurine.
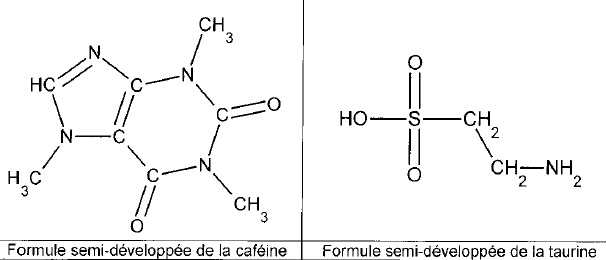
2.1. Dessiner la cafine en utilsant un autre mode de représentation dont on précisera le nom.
Formule topologique de la caféine :
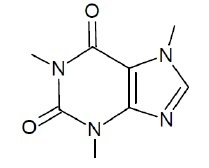
Addition du dihydrogène sur une double liaison C=N ; une double liaison
disparaît et deux liaisons simples sont créées.
2.2. Prévoir le nombre de signaux présents dans le spectre RMN de la cafèine ainsi que leur multiplicité. Justifier.
Les trois groupes méthyle donnent chacun un singulet ( les atomes voisins ne portent pas d'hydrogène).
Le proton N=CH donne également un singulet.
Donc 4 signaux.
2.3. Montrer que le spectre IR ci-dessous peut être celui de la caféine
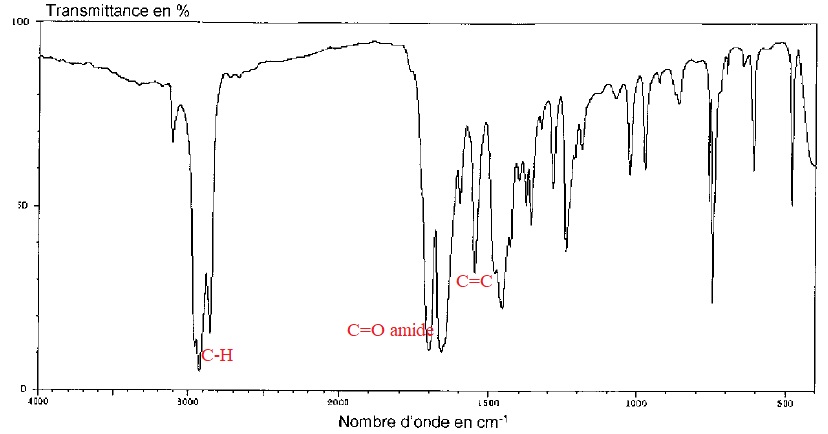
2.4. La spectroscopie IR permet-elle de distinguer la caféine de la taurine ? Argumenter.
Oui. Le spectre de la taurine ne présente pas de bande vers 1650 - 1740 cm-1 ( pas de groupe C=O) et présente un pic vers 1200 - 1350 cm-1 ( liaison S=O). De plus le spectre de la taurine présente une large bande vers 3000 cm-1 ( OH lié).
|
|
|