Physique
chimie, radiographie, cure thermale,
Bac STI2D STL biotechnologie Métropole 09 / 2018
En
poursuivant votre navigation sur ce site, vous acceptez l’utilisation
de Cookies vous proposant des publicités adaptées à vos centres
d’intérêts.
|
|
|
|
Partie
A - La radiographie.
A.1. Ondes
électromagnétiques et radiographie.
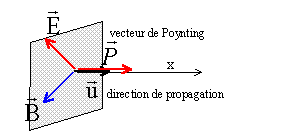
A.1.1. Rappeler la
structure d’une onde électromagnétique.
Une onde électromagnétique comporte un champ électrique et un champ
magnétique oscillant à la même fréquence. Ces champs, perpendiculaires
l'un par rapport à l'autre, se propage selon une direction orthogonale.
Cette onde se propage avec une vitesse qui dépend du milieu.
A.1.2.
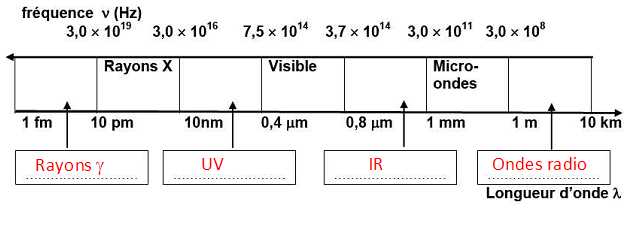
Compléter le spectre des ondes électromagnétiques en associant à chaque
numéro le domaine des ondes électromagnétiques correspondant et choisi
parmi les suivants : micro-ondes, lumière visible, ondes hertziennes,
ultraviolets, rayons gamma, infrarouges.
A.1.4. Expliquer les variations de
contraste observées sur l’image obtenue.
La radiographie enregistre l'image d'un
corps traversé par un faisceau de rayons X. Suivant la constitution du
corps, les rayons X sont plus ou moins absorbés et le film
photographique, placé derrière le corps radiographié, est ainsi plus ou
moins impressionné.
Les os absorbent fortemment les rayons X et apparaissent en blanc.
Les tissus absorbent peu
les rayons X et apparaissent en gris.
A.1.5. L’appareil radiographique
produit des rayons X d’énergie E = 120 keV.
A.1.5.1. Calculer la fréquence n des photons émis lors de
l’examen radiographique.
E = 1,2 105 x1,6 10-19 =1,92 10-14 J.
Fréquence n = E /
h = 1,92 10-14 / (6,62 10-34) = 2,90 1019
Hz.
A.1.5.2. Déterminer la longueur
d’onde dans le vide l
des photons émis et vérifier qu’ils appartiennent au domaine des rayons X.
l = c
/ n = 3,00 108
/ (2,90 1019) =1,03 10-11 m.
Cette valeur est comprise entre 10-8 m et 10-12 m
; ces photons appartiennent au domaine des rayons X.
A.2. Dose de rayonnement X reçue par
madame K
L’appareil radiographique
émet par seconde 8,0 × 109 photons d’énergie E = 120 keV
chacun.
A.2.1. Montrer que la patiente
reçoit une dose D d’environ 90 μGy lors de cette radiographie qui dure Δt = 10 s
sachant que la masse m de la partie du corps
irradiée est d’environ 17
kg.
Energie totale reçue : E = 1,20 105 x1,6 10-19
x8,0 109 x10 = 1,536 10-3 J.
Dose reçue = E / m = 1,536 10-3 / 17 = 9,04 10-5
Gy ~90 µGy..
A.2.2. Vérifier par le calcul que la
dose équivalente reçue ED respecte la limite autorisée.
ED = 9,04 10-5 x0,12 = 1,08 10-5 Sv.
Cette valeur est très inférieure à 1 mSv, dose anuelle maximale.
A.3. Radioprotection du personnel
médical
Pour se protéger, la
manipulatrice radio porte un tablier contenant du plomb. L’absorption
d’un rayonnement
électromagnétique par un écran dépend de l’énergie des photons émis, du
matériau utilisé et de
l’épaisseur de l’écran.
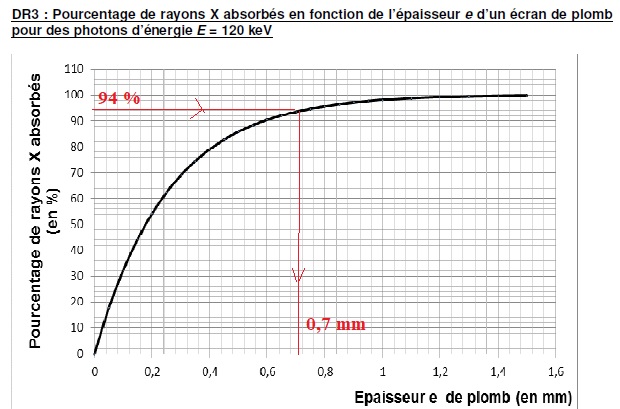
Le document suivant donne
le pourcentage de rayonnement X absorbé en fonction de l’épaisseur e d’un écran de plomb pour des
photons d’énergie E = 120 keV. Déterminer l’épaisseur e de plomb du
tablier utilisé pour obtenir un pourcentage d’absorption de 94 %.
|
|
|
|
|
PARTIE
B : Le trajet jusqu’au centre thermal.
Madame K vient d’acheter récemment une voiture diesel. Elle a remarqué
que sa consommation moyenne est de 3,30 L de gazole pour 100 kilomètres
parcourus et souhaite vérifier si cette dernière satisfait à l’objectif
fixé par l’Union européenne pour 2020 concernant la pollution au CO2,
à savoir une émission de 95 g de CO2 produit par kilomètre
parcouru.
Le gazole est un carburant fossile constitué d’un mélange de différents
composés miscibles. Pour simplifier, on l’assimilera à un alcane de
formule brute C21H44.
Donnée : masse volumique du gazole : r = 845 g · L-1 ;
B.1.1. Déterminer
le volume Vg de gazole consommé par kilomètre parcouru.
3,3 / 100 = 0,033 L.
B.1.2. En déduire
que la quantité de matière n de gazole consommé par kilomètre parcouru
est de 9,42 × 10-2 mol.
masse de 0,033 L de gazole : m = 0,033 x 845 = 27,885 g.
Masse molaire de C21H44.
M = 21 x12 +44 = 296g / mol.
Quantité de matière de gazol n = m / M = 27,885 / 296 ~9,42 × 10-2
mol.
B.1.3. Recopier sur la copie
l’équation de combustion du gazole dans le dioxygène de l’air et
l’équilibrer.
C21H44 + 32. O2
---> 21 CO2 +
22. H2O
B.1.4. Déterminer
la quantité de matière n(CO2) de dioxyde de carbone rejeté
pour un parcours d’un kilomètre.
n(CO2)=
21 x 4,92 10-2 =1,98 mol.
B.1.5. La voiture de madame K
satisfait-elle l’objectif fixé
n(CO2)
x M(CO2)=1,98
x 44 ~87 g, valeur inférieure à 95. l'objectif est respecté.
|
|
PARTIE C : Siège élévateur pour personne à
mobilité réduite
L’accès à la piscine du centre thermal a été aménagé pour permettre aux
personnes à mobilité réduite d’accéder au bassin. Un moteur alimenté
par une
batterie permet de déplacer verticalement une plateforme élévatrice.
Données constructeur :
- La plateforme de masse à vide m = 53,0 kg peut supporter une charge
de masse maximale de 150 kg et permet de descendre d’une hauteur h =
1,44 m.
- La durée totale de montée ou de descente est de Δt = 18 s.
- La batterie délivre une puissance moyenne P = 80 W pour un
fonctionnement à vide (sans charge).
Un watt·heure vaut 3 600 joules : 1 W h = 3 600 J
On donne l’intensité de pesanteur terrestre : g = 9,81 N · kg-1.
Le document ci-dessous décrit l’évolution de la vitesse de la
plateforme en fonction du temps :
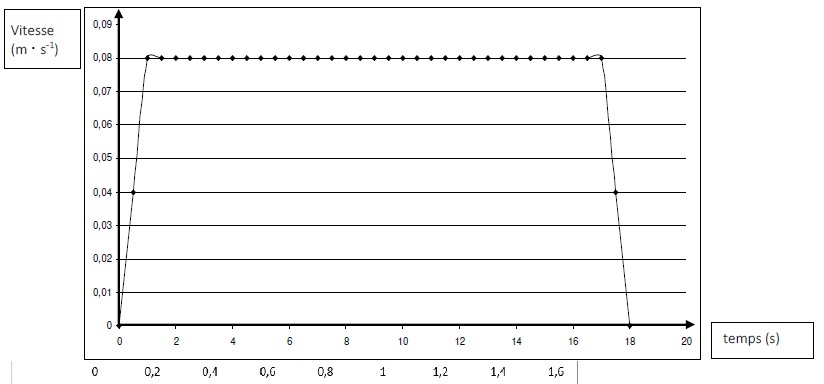
Dans toute cette partie, on étudie le mouvement de la plateforme à vide.
C.1.1. Vérifier que
la vitesse maximale vmax du siège, lue sur le graphe, est
compatible avec les données du constructeur sur la durée de montée.
h / Dt = 1,44 /
18 =0,08 m /s =vmax.
C.1.2. Sur le
graphe, identifier les phases de démarrage et d’arrêt. Comment peut-on
qualifier le mouvement entre ces deux phases ?
Phase de démarrage : entre 0 et 1 s ; phase d'arrêt : entre 17 et 18 s.
Entre ces deux phases le mouvement est uniforme ( la valeur de la
vitesse est constante).
C.1.3. Citer les
forces appliquées sur la plateforme pendant une montée.
Poids, poussée d'Archimède due à l'eau et force motrice exercée par le
moteur.
C.1.4. Que peut-on
dire de la résultante de ces forces entre t1 = 1,0 s et t2
= 17 s ?
Le mouvement étant rectiligne uniforme, la somme vectorielle des forces
appliquées sur la plate-forme est nulle.
C.1.5. Déterminer
la variation de l’énergie mécanique ΔEm de la plateforme
lors d’une seule montée du siège.
L'énergie cinétique est nulle ( vitesse nulle au départ et à la fin).
L'origine de l'énergie potentielle étant prise au point le plus bas, la
variation d'énergie potentielle vaut :
ΔEm = 0-mgh = -53x9,81 x1,44 ~749 ~-7,5 102
J.
C.1.6. En
raisonnant sur les unités, indiquer parmi les 3 expressions proposées
ci-dessous la relation correcte entre l’énergie et la puissance :
E = P · Δt ; E = P / Dt ; E = P2 · Δt
C.1.7. Déterminer
l’énergie E fournie par la batterie lors d’une seule montée du siège.
P Dt = 80 x 18
=1,44 103 J.
C.1.8. Expliquer
pourquoi l’énergie E fournie par la batterie est supérieure à l’énergie
mécanique reçue par la plateforme.
Une partie de l'énergie est dissipée sous forme thermique ( frottement
).
PARTIE D : Eau thermale et
soins
D.1. À propos de
l’eau thermale
L’eau thermale est une eau de type sulfurée sodique. Elle se
caractérise principalement par :
- une faible minéralisation (0,18 g · L-1),
- la présence de sulfures sous les formes de sulfure d’hydrogène H2S,
d’ions hydrogénosulfure HS- ou d’ions sulfure S2-,
- la dominance de la teneur en sodium (ions Na+).
Données :
masse volumique de l’eau : reau
liquide = 1,0 × 103 g · L-1 ;
pH de l’eau thermale : pH = 9,3 ;
température de l’eau thermale : environ 25°C.
- Le sulfure d'hydrogène est un composé chimique de formule H2S.
C'est un gaz acide, incolore, à l'odeur nauséabonde d'oeuf pourri et
très toxique par inhalation à partir d’un seuil de 14 mg · m−3.
Il réagit avec les solutions aqueuses basiques et les métaux tels que
l'argent.
- Couples acide / base : H2S / HS- ; HS-
/ S2-.
D.1.1. Citer deux
méthodes permettant de mesurer le pH d’une solution.
L'Indicateur de papier pH donne un valeur approximative.
Le pHmètre donne une valeur précise.
D.1.2. L’eau
thermale est-elle acide, basique ou neutre ? Justifier la réponse.
A 25°C, l'eau est basique, son pH ( 9,3) est supérieur à 7.
D.1.3. Déterminer
la concentration en ions oxonium H3O+ dans cette
eau thermale et en déduire la concentration en ions hydroxyde HO-.
[ H3O+] = 10-pH = 10-9,3 =
5,0 10-10 mol/ L.
[HO ] = 10-14 / [ H3O+] =10-14
/ ( 5,0 10-10)=2,0 10-5 mol /L.
D.1.4. Les produits ménagers
anticalcaires contiennent des espèces chimiques acides.
D.1.4.1 Donner la
définition d’un acide selon la théorie de Brönsted.
Un acide est une espèce, ion ou molécule, susceptible de céder un
proton H+.
D.1.4.2. Écrire
l’équation chimique de la réaction entre l’ion hydrogénosulfure HS-
et l’ion oxonium H3O+, espèce acide du couple H3O+/H2O.
HS- + H3O+ =H2O
+ H2S..
D.1.4.3. À quel désagrément
s’expose-t-on en ajoutant un produit ménager anticalcaire avec de l’eau
thermale ? Justifier.
Dégagement de H2S,
gaz acide, incolore, à l'odeur nauséabonde d'oeuf pourri et très
toxique par inhalation.
D.2. Un exemple de soin
ORL : douche nasale
- Le dispositif est composé :
- d’une cuve en verre de volume V = 3,0 L, munie à sa base d’un tuyau
souple dont l’autre extrémité est raccordée à
un tube en inox permettant de brancher le tube nasal du patient.
- d’un robinet R en inox qui permet de régler le débit de l’eau
thermale isotonique*.
*Eau thermale isotonique : eau thermale dans laquelle on a ajouté m =
10,0 g de sel par litre d’eau thermale.
- La prescription du médecin : Douche nasale d’eau thermale isotonique
de deux litres :
- un litre par narine pendant quatre minutes.
Éviter tout mouchage violent pendant la douche nasale et ainsi que dans
la demi-heure qui suit.
- Données : masse volumique eau thermale isotonique : r = 1,01 × 103
kg · m-3 ;
pression atmosphérique : PA = Patm = 1,02 × 105
Pa ; |

|
D.2.1. En
appliquant le principe fondamental de l’hydrostatique entre les points
A et B, déterminer la pression PB au point B lorsque le
robinet du dispositif est fermé.
PB -PA = r
g AB =1,01 103 x9,81
x0,25 = 2477 Pa ;
PB = 1,02 105 + 2477 = 1,045 105 ~1,04
105 Pa.
D.2.2.
Madame K ouvre le robinet R pour effectuer son soin ORL.
D.2.2.1 D’après la
prescription, montrer que le débit volumique de l’eau thermale
isotonique pour ce soin est Dv = 4,2 × 10-6 m3
· s-1.
1 L = 10-3 m3 ; 4 min = 4 x60 = 240 s.
10-3 / 240 = 4,2 ×
10-6 m3 · s-1.
D.2.2.2. Sachant que la vitesse
d’écoulement vA au point A est de 5,3 × 10-4 m · s-1,
déterminer le diamètre de la cuve dA au point A.
Section du tube ; S = Dv / vA = 4,2 × 10-6 / (5,3 × 10-4 ) =7,924 10-3 m2 ;
dA = (4 x7,924 10-3 / 3,14)½ ~0,10 m.
D.3. Un autre soin thermal
: l’aérobain
Ce soin consiste à immerger le corps de la patiente dans une baignoire
à bulles remplie d’eau thermale à une température q1 = 36°C durant
Δt = 10 min. Le volume d’eau thermale dans la baignoire est Vb
= 240 L.
Avant que madame K s’immerge, on vérifie la température du bain : le
thermomètre affiche q2
= 38°C, il est donc nécessaire d’ajouter une masse mf d’eau
froide que l’on se propose de déterminer.
Données : capacité thermique massique de l’eau ceau = 4,2 ×
103 J · kg−1 · °C−1 ;
masse volumique de l’eau : r =
1 000 kg · m-3 .
On rappelle que l’énergie échangée sous forme de chaleur Q lors d’une
variation de température Dq pour un corps de masse m
et de capacité thermique massique c s’écrit : Q = m · c · Dq.
D.3.1. Calculer
l’énergie QP perdue par l’eau présente au départ dans le
bain pour passer de la température 38°C à la température 36°C.
QP = 240 x4,2 103
x(-2) = -2,016 106 ~ -2,0 106 J.
D.3.2. En négligeant les pertes
thermiques, montrer que la masse mf d’eau froide à rajouter
au bain de madame K pour le refroidir est de 25 kg.
Energie gagnée par l'eau froide à 17°C : mf x4,2 103
(36-17) = 7,98 104 mf J.
mf = 2,016 106
/ (7,98 104) ~25 kg.
D.3.3. Le débit du robinet d’eau de
la baignoire étant Dvrob = 20 L · min-1, pendant
quelle durée Δt le robinet d’eau froide doit-il rester ouvert pour
refroidir à 36°C l’eau du bain de madame K ?
25 / 20 = 1,25 min = 1 min 15 s.
|
|