Les fresques
de Bamiyan, Bac S Polynésie 2018
En
poursuivant votre navigation sur ce site, vous acceptez l’utilisation
de Cookies vous proposant des publicités adaptées à vos centres
d’intérêts.
|
|
.
.
|
|
Dans
la région de Bamiyan, des chercheurs ont découvert des fresques bien
conservées. Des prélèvements ont révélés l'existence d'huile de noix.
Les huiles de lin et de noix sont siccatives, elles peuvent former un
film résistant et continu lorsqu'elles sont exposées à l'air en couche
mince. Cette propriété est due à la présence de doubles liaisons dans
les composés insaturés présents dans ces huiles. La sicativité d'une
huile est mesurée par l'indice d'iode de l'huile.
Détermination expérimentale de l'indice d'iode d'une huile.
On appelle indice d'iode la masse de dihalogène, exprimée en gramme de
diiode, qui pourrait se fixer sur 100 g de substance étudiée. le diiode
se fixant lentement sur les doubles liaisons, on le remplace par le
chlorure d'iode ICl. En milieu non aquex, le chlorure d'iode se fixe
sur les doubles liaisons suivant la réaction :
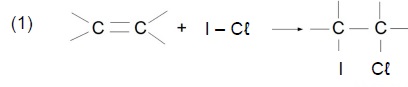
Le chlorure d'iode ( réactif de Wijs) est utilisé en excès. ICl restant est transformé totalement en diiode.
(2) ICl restant + I- excès ---> I2 + Cl-.
Le diiode formé est titré par les ions thiosulfate.
(3) I2 + 2S2O32- ---> 2I- +S4O62-.
Protocole expérimental.
Echantillon 1 : dans un erlenmeyer sec de 250 mL introduire dans l'ordre :
0,30 g d'huile d'olive.
25 mL de cyclohexane à l'aide d'une éprouvette graduée.
10,0 mL de réactif de Wijs prélevé sous la hotte à l'aide d'une pipette jaugée.
Boucher, agiter, placer à l'obscurité pendant 45 minutes avant traitement.
Echantillon 2 : dans un erlenmeyer sec de 250 mL introduire dans l'ordre :
25 mL de cyclohexane à l'aide d'une éprouvette graduée.
10,0 mL de réactif de Wijs prélevé sous la hotte à l'aide d'une pipette jaugée.
Boucher, agiter, et traiter l'échantillon.
Traitement des deux échantillons.
Dans chaque échantillon ajouter :
100 mL d'eau distillée, 15 mL d'iodure de potassium en excès.
Agiter, attendre quelques minutes à l'obscurité.
Titrer chaque échantillon, en agitant, par une solution de thiosulfate
de sodium ( concentration c = 0,200 mol /L). Ajouter l'empois d'amidon
en fin de titrage pour repérer avec précision l'équivalence (
disparitio du diiode).
Le traitement de l'échantillon 2 permet de connaître la quantité de
matière initiale de chlorure d'iode contenue dans 10,0 mL de réactif de
Wijs.
VE1 = 11,9 mL ; VE2 = 22,9 mL.
Questions préalables.
1. Montrer que la quantité de matière de diiode formé par la réaction (2) est égale à ½cVE.
D'après
les nombres stoechiométriques de (3) : quantité de matière de diiode =
0,5 fois la quantité de matière d'ion thiosulfate à
l'équivalence = ½cVE2.
Quantité de matière de diiode formé en (2) : n = ½cVE2 = 0,5 x 0,200 x 22,9 = 2,29 mmol.
2.
Déterminer à partir du traitement de l'échantillon 2, la quantité de
matière initiale de chlorure d'iode contenue dans 10,0 mL de
réactif de Wijs.
La quantité de matière de ICl est égale à celle de diiode formé en (2).
2,29 mmol.
|
|
|
|
|
Problème.
Les
peintres des fresques disposaient également d'huile d'olive.
Auraient-ils pu remplacer l'huile de noix par de l'huile d'olive
pour réaliser ces fresques ?
Echantillon 1 : quantité de matière de diiode formé en (2) = quantité de matière de ICl en excès.
½cVE1 = 0,5 x 0,200 x 11,9 = 1,19 mmol.
Quantité de matière de chlorure d'iode ayant réagi avec les doubles liaisons de l'huile d'olive :
2,29 -1,19 = 1,10 mmol.
La quantité de matière de ICl qui se fixe est égale à la quantité de
matière de diiode qui se fixerait si le diiode était utilisé comme
réactif.
Masse de diiode correspondante : 1,10 M(I2) = 1,10 x 254 = 279,4 mg ~ 0,279 g.
Indice d'iode de l'huile d'olive :
0,279 x 100 / 0,30 ~93,1 .
Cette valeur étant inférieure à 110, l'huile d'olive est non siccative. Elle ne peut pas remplacer l'huile de noix.
Quantité de matière de ICl ayant réagi avec l'huile d'olive :
2,29 -1,19 = 1,10 mmol.
|
|
.
|
|