La saveur umami.
bac S Pondichéry 2017.
En
poursuivant votre navigation sur ce site, vous acceptez l’utilisation
de Cookies vous proposant des publicités adaptées à vos centres
d’intérêts.
|
|
|
|
|
|
|
|
1. L'acide glutamique.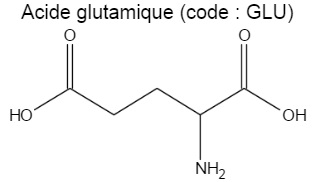
1.1. Justifier que
cet acide est un acide aminé.
Cet acide posséde une fonction acide carboxylique et une fonction amine.
1.2. Indiquer si
les molécules A et B, puis A et C, représentées ci-dessous sont
identiques, énantiomères ou diastéréoisomères.
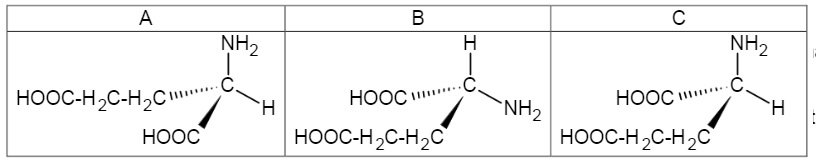
A et C sont
énantiomères : on a permutté HOOC et CH2-CH2-COOH.
B et C sont énantiomères : on a permutté H et NH2.
Par conséquent A et B sont identiques.
1.3 Synthèse de l'acide
glutamique.
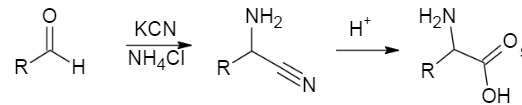
1.3.a. Dans le cas
de l'acide glutamique, donner la formule semi-développée de R.
CH2-CH2-COOH.
|
|
|
Une
étape du mécanisme réactionnel est donnée ci-dessous.
1.3.b. Représenter
les flèches courbes qui rendent compte de cette étape.
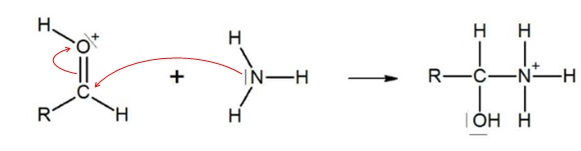
1.3.c Associer à
cette étape une catégorie de réaction en justifiant..
Addition
de l'ammoniac NH3 sur la double liaison C=O+.
Une double liaison disparaît, il se forme une liaison simple. A partir
de deux réactifs, on obtient un seul produit.
|
|
.
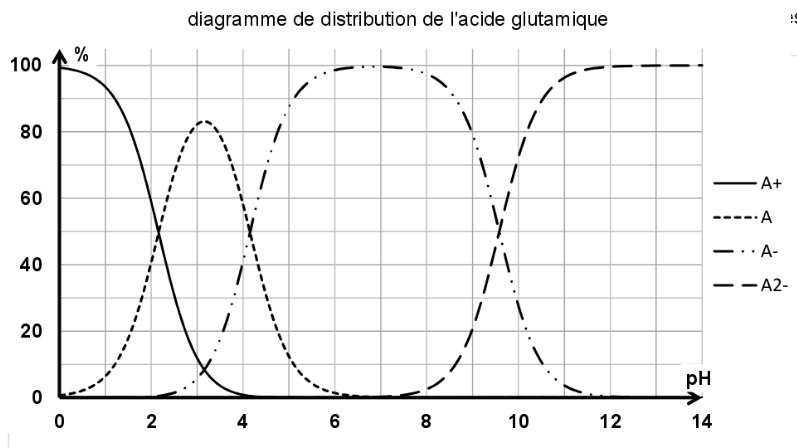
A pH = 12, GLU est sous forme d'ion négatif ( deux charges négatives);
à pH = 7 il est sous forme d'ion négatif et à pH = 2 elle est
majoritairement sous forme de cation
positif.
A pH =7, la sérine neutre ne migre pas, tandis que GLU ( négatif) migre
vers le pôle positif.
2.5. Suite à la
séparation de SER et GLU peut-on distinguer SER et GLU en spectroscopie
IR ?
Non, les deux acides aminés présentent les mêmes groupes
fonctionnels ( acide carboxylique et amine). Quand au signal de
l'alcool OH lié de la sérine, il recouvre celui de OH lié ( acide
carboxylique).
|
|