Le très grand
télescope,
bac
S Antilles 2017 .
|
|
En
poursuivant votre navigation sur ce site, vous acceptez l’utilisation
de Cookies vous proposant des publicités adaptées à vos centres
d’intérêts.
|
|
|
|
|
|
|
|
L'objectif
de cet exercice est de comprendre pourquoi les scientifiques
construisent des télescopes ayant des diamètres de plus en plus grands.
1. Un télescope du VLT.
Lorsqu'on
observe une étoile à travers un télescope, l'image apparaît sous la
forme d'une tache, dont la dimension est liée aux défauts que présente
l'instrument, tels que :
- la sensibilité aux fluctuations atmosphériques ;
- la diffraction par l'ouverture limitée de l'instrument.
On étudie l'influence du diamètre de l'ouverture circulaire du
télescope sur la qualité de l'image formée. Pour cela on réalise le
montage suivant, dans lequel le laser correspond à l'étoile et le
miroir du télescope est modélisé par une ouverture circulaire de
diamètre a produisant un phénomène de diffraction.
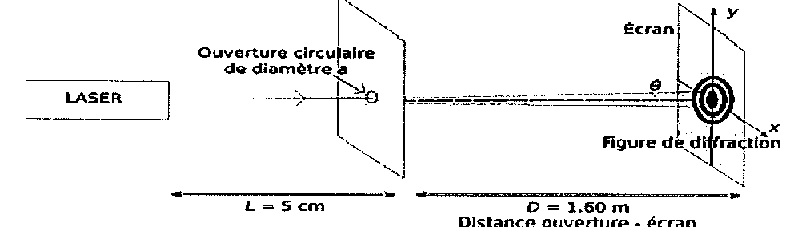
Document1. Figures
de diffraction : intensité lumineuse obtenue pour des ouvertures
circulaires de diamètres 0,2 mm et 0,4 mm.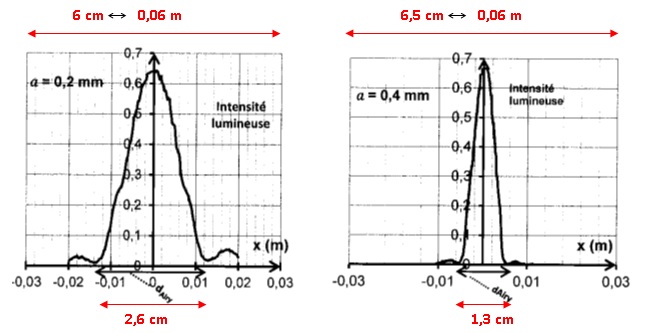 1.1. Décrire le phénomène de
diffraction. Dans quelle condition ce phénomène est-il observable.
1.1. Décrire le phénomène de
diffraction. Dans quelle condition ce phénomène est-il observable.
On appelle diffraction, le changement de direction de propagation d'une
onde, sans modification de sa longueur d'onde, lorsque celle-ci
rencontre un obstacle ou une ouverture dont les dimensions sont du même
ordre de grandeur que la longueur d'onde. Le phénomène est d'autant
plus marqué que le rapport de la longueur d'onde sur la dimension de
l'ouverture ou de l'obsatcle est grand.
1.2. Quel caractère
de la lumière est mis en évidence par l'apparition d'une figure de
diffraction ?
Le caractère ondulatoire de la lumière est mis en évidence.
1.3. A partir des
résultats expérimentaux, déterminer la valeur du diamètre dAiry
de chaque tache observée pour les deux ouvertures. Comment évolue le
diamètre de la tache quand l'ouverture du télescope augmente ?
a = 0,02 mm :
dAiry =2,6 x0,06 /6 = 0,026 m = 2,6 cm.
a = 0,04 mm : dAiry
=1,3 x0,06 /6,5 = 0,012 m = 1,2 cm.
Le
diamètre de la tache diminue quand l'ouverture du télescope
augmente.
|
....
.....
|
La qualité d'un télescope est
caractérisée par son pouvoir de
résolution : c'est à dire sa capacité à séparer deux objets très
proches comme un étoile double par exemple.
L'observation, par un télescope des deux étoiles, d'une étoile double,
séparées d'un angle q,
donne deux taches circulaires sur l'écran si l'angle q sous lequel elles sont
vues, est supérieur à une valeur limite qmin = 1,22 l / a.
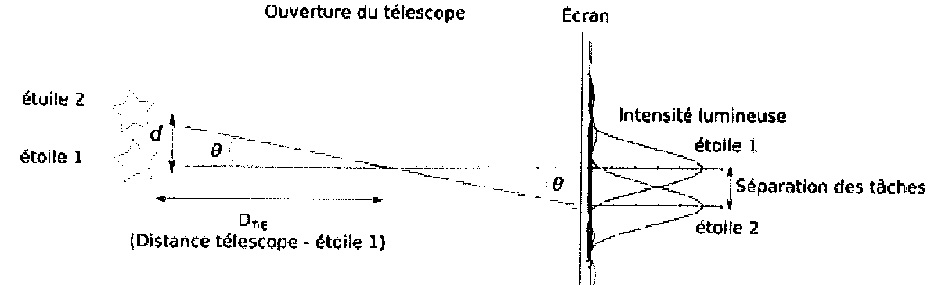
Dans la suite de
l'exercice, les objets observés étant très éloignés, l'angle q est petit et on peut
écrire tan q ~ q radian.
Données :
distance terre-lune : DTL = 3,8 108 m.
La vision humaine a une sensibilité maximale, en vision diurne, pour un
rayonnement de longueur d'onde voisine de 560 nm.
1.4.
On considère deux objets placés sur la Lune à une distance d l'un de
l'autre..Déterminer la valeur minimale de la distance d pour que les
deux objets puissent être séparés par :
- un télescope terrestre de diamètre 4,0 m ;
un télescope du VLT ( diamètre 8,2 m).
q ~d
/ DTL ; qmin = 1,22 l / a.
Dans le cas limite : 1,22 l / a = dmini / DTL
;
dmini = 1,22 l DTL / a
=1,22 x560 10-9 x3,8 108 / 4,0 = 64,9 ~65 m pour
le télescpoe terrestre.
dmini = 1,22 l DTL / a
=1,22 x560 10-9 x3,8 108 / 8,2 = 31,6 ~32 m pour
le télescpoe du VLT.
1.5. Justifier les
choix des scientifiques en termes de matériel et de leur implantation.
Il faut des télescope de grande ouverture pour augmenter le pouvoir de
résolution.
Il faut les placer dans des régions où l'atmosphère est très stable.
II. Entretien des miroirs
du VLT.
Le miroir de 50 m2 de surface est débarassé de sa couche
d'aluminium de 80 nm d'épaisseur avec de l'eau, de l'acide et du
sulfate de cuivre. L'opération consomme environ 3000 litres d'eau. le
miroir est ensuite recouvert d'une nouvelle couche d'aluminium
identique à la précédente. D'après l'émission France 5 Superstructures
SOS - le miroir des étoiles.
Etiquette du flacon d'acide chlorhydrique utilisé.
M = 36,45 g / mol ; 37 % en masse ; d = 1,188.
|
|
|
2.1.
Etape 1 : élimination de la couche d'aluminium..
Seul l'acide chlorhydrique attaque l'aluminium.
2Al(s) +6H3O+aq ---> 2Al3+aq +3H2(g)
+6H2O(l).
2.1.1 A partir des
demi-équations électroniques des couples oxydant / réducteur, retrouver
l'équation de la réaction entre l'aluminium et les ions oxonium.
Couples Al3+aq / Al (s) : 2Al(s) = 2Al3+aq +6e-.
Couple H3O+aq / H2(g) : 6H3O+aq +6e-
=3 H2(g) +6H2O(l).
Ajouter et simplifier : 6H3O+aq +6e-
+
2Al(s)=3
H2(g) +6H2O(l) +2Al3+aq +6e-.
6H3O+aq
+
2Al(s)=3
H2(g) +6H2O(l) +2Al3+aq .
2.1.2.
De quel type de réaction s'agit-il ? Quel est le rôle de l'aluminium et
celui des ions oxonium ? Justifier.
C'est une réaction d'oxydo-réduction.
L'aluminium cède des électrons,
c'est un réducteur qui s'oxyde.
Les ions oxonium gagnent des
électrons, c'est un oxydant
qui se réduit.
2.1.3 Quel est le
volume d'aluminium VAl déposé sur le miroir ? Vérifier que
la quantité de matière d'aluminium présente dans cette couche est nAl
= 0,40 mol.
VAl = Surface fois épaisseur = 50 x80 10-9 = 4,0
10-6 m3.
Masse volumique de l'aluminium 2,7 106 g m-3.
Masse correspondante : m = 4,0 10-6 x 2,7 106 =
10,8 g.
nAl = m / M(Al) = 10,8 / 27 =0,40 mol.
2.1.4. Déterminer
la quantité de matière d'ion oxonium nécessaire à l'élimination de la
couche d'aluminium.
D'après les nombres stoechiométriques de l'équation, il faut 0,40 x3 = 1,2 mol d'ion oxonium.
2.1.5. Montrer que
la concentration Ca de la solution d'acide chlorhydrique est
de l'ordre de 12 mol/L.
Masse de 1 L de cette solution : 1,188 kg.
Masse d'acide : m=0,37 x1,188 ~0,440 kg = 440 g.
Quantité de matière d'acide : m / M(HCl) = 440 / 36,5 ~ 12 mol dans 1 L.
2.1.6. On souhaite
préparer une solution 100 fois moins concentrée. Proposer un protocole
expérimental pour préparer 1,00 L de solution.
A l'aide d'une pipette jaugée prélever 10,0 mL de la solution mère.
Verser dans une fiole jaugée de 1,00 L contenant un tiers d'eau
distillée.
Compléter avec de l'eau distillée jusqu'au trait de jauge.
Boucher et agiter pour rendre homogène.
2.1.7. Quel volume V1
de la solutiondiluée est nécessaire pour éliminer la couche d'aluminium
?
Il faut 1,2 mol d'ion oxonium ; V1 = n / C1 =1,2
/ 0,12 = 10 L.
|
|
|
|
Etape 2 :Dépôt d'une nouvelle couche
d'aluminium.
Principe de la pulvérisation cayhodique.
L'application d'une tension électrique permet la création
d'un plasma d'argon : un électron d'une couche externe de l'atome
d'atgon Ar peut être arraché lors d'une collision entre un atome
d'argon et un électron incident. Ce mécanisme est modélisé par :
Ar +e-incident --> Ar+ +e-incident
+e-émis.
Sous l'effet du champ électrique, les ions positifs Ar+ du
plasma se trouvent attirés par la cathode en aluminium et entrent en
collision avec cette dernière, ce qui provoque la pulvérisation des
atomes d'aluminium qui vient se déposer sur le miroir.
Masse de l'électron m = 9,11 10-31 kg ; énergie d'ionisation
de l'atome d'argon : E1 = 15,8 eV.
2.2.1.. L'énergie
nécessaire à
l'ionisation de l'atome d'argon est apportée par l'énergie cinétique de
l'électron incident. Déterminer la vitesse de l'électron incident et
commenter l'ordre de grandeur obtenu.
E1 = 15,8 eV soit 15,8 x1,60 10-19 = 2,528 10-18
J.
E1 = ½mv2 ; v = (2E1 / m)½
=(2 x2,528 10-18 / (9,11 10-31))½=2,36 106 m /s.
Cette valeur élevée reste inférieure à 10 % de la vitesse de la lumière
dans le vide : l'électron n'est pas relativiste.
2.2.2.
Si l'énergie transférée par l'électron incident, lors de la collision,
n'est pas suffisante pour l'ionisation, un électron de la couche
externe de l'atome d'argon peut passer à un niveau excité. Dans le cas
d'un transfert d'énergie de 11,6 eV, faire un schéma énergétique et
indiquer par une flèche la transition se produisant. Quelle est la
nature du rayonnement ( IR, visible, UV ) émis par l'électron quand il
revient à son état fondamental ?
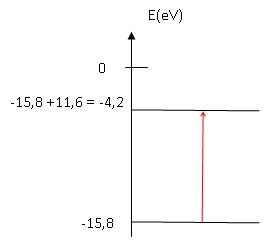
DE = h
c / l ; l = 6,63 10-34
x3,00 108 /(11,6 x1,60 10-19)=1,07 10-7
m = 107 nm.
Cette valeur, inférieure à 400 nm, appartient au domaine UV.
|
|