QCM
chimie.
Concours kinť EFOM 2016.
En poursuivant votre navigation sur ce site, vous acceptez l’utilisation de Cookies vous proposant des publicitťs adaptťes ŗ vos centres d’intťrÍts.
|
|
.
.
|
|
|
|
|
|
|
|
Exercice 1.
L'aspartame
est un ťdulcorant artficiel prťsent dans le soda (S). Son pouvoir
sucrant est environ 200 fois supťrieur ŗ celui du saccharose. La dose
maximale admissible en aspartame est fixťe ŗ 40 mg par kilogramme
de masse corporelle par jour. Cette molťcule est un dipeptide obtenu
par formation d'une liaison peptidique entre deux acides aminťs.
Teneur en aspartame du soda : t = 0,50 mg /L.
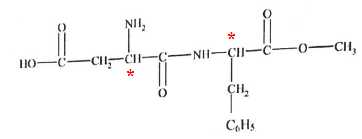
A. L'aspartame possŤde entre autre une fonction amine. Vrai.
B. Il existe 4 stťrťoisomŤres de configuration de l'aspartame. Vrai.
L'existence de deux atomes de carbone asymťtriques conduit ŗ 4 stťrťoisomŤres.
C. Il existe un unique couple d'ťnantiomŤres de l'aspartame. Faux.
D. Un adolescent de 50 kg pourrait boire jusq'ŗ 1000 L de soda par jour sans dťpasser la dose maximale admissible. Faux.
50*40 =2 000 mg par jour soit boire : 2000 / 0,50 = 4000 L par jour.
Exercice 2.
Le vert de bromocrťsol est un indicateur colorť de pH dont les
formes acide et base conjuguťes ont des couleurs diffťrentes en
solution aqueuse. Laforme acide, notťe HIn est de couleur jaune en
solution aqueuse alors que la teinte sensible prise par
l'indicateur colorť entre pH=3,8 et pH = 5,4 est verte. Une ťtude
expťrimentale menťe ŗ 25įC permet de tracer la courbe p(HIn) = f(pH)
donnťe ci-aprŤs. Elle reprťsente l'ťvolution du pourcentage molaire de
la forme acide de l'indicateur colorť en fonction du pH de la solution
aqueuse dans laquelle elle se trouve.
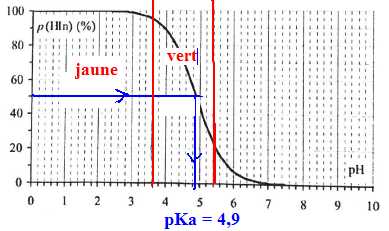
A. A 25įC, une solution de pH=6,0 est acide. Vrai.
B. A 25įC, le pKa du couple HIn / In- du vert de bromocrťsol est de 4,9. Vrai.
C. A pH = 6 et ŗ 25įC, une solution contenant comme unique indicateur colorť le vert de bromocrťsol est jaune.
Faux.
D. La forme basique In- du vert de bromocrťsol est bleue en solution aqueuse. Vrai.
Exercice 3.
On rťalise le titrage par suivi pHmťtrique d'un volume V =20,0 mL d'une solution aqueuse (S) d'ťthanamine C2H5-NH2 par l'acide chlorhydrique de concentration molaire c = 1,0 10-2 mol/L. On donne la courbe obtenue. Couple C2H5-NH3+ / C2H5-NH2 : pKa = 10,7 ŗ 25įC.
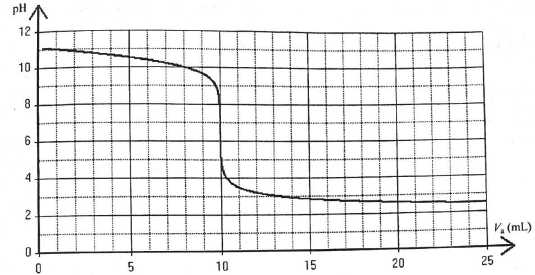
A. Le pH de la solution titrante est 2,5. Faux.
pH = -log c = -log 0,010 = 2.
B. Avant l'ajout d'acide chlorhydrique, la solution (S) ŗ titrer contient dťja des ions ťthylammonium C2H5-NH3+ aq . Vrai.
pH = pKa + log( [C2H5-NH2 aq] /[C2H5-NH3+ aq]) ;
log( [C2H5-NH2 aq] /[C2H5-NH3+ aq]) = 11-10,7 = 0,3 ; [C2H5-NH2 aq] /[C2H5-NH3+ aq] ~ 2
[C2H5-NH3+ aq] = 0,5 [C2H5-NH2 aq].
C. Tant que le mťlange est basique, c'est l'ťthanamine qui prťdomine devant l'ion ťtylammonium. Faux.
Tant que le pH du mťlange est supťrieur ŗ pKa =10,7, c'est l'ťthanamine qui prťdomine devant l'ion ťtylammonium.
D. La concentration molaire en ťthanamine apportťe est c' = 5,0 10-3 mol/L. Vrai.
A l'ťquivalence cVE = c' V ; VE = 10 mL.
c' = cVE / V = 1,00 10-2 *10 / 20 = 5,0 10-3 mol/L.
Exercice
4.
La
pezmiŤre ťtape du mťcanisme de la rťaction de saponification d'un
ester fait intervenir un ion hydrosyde. L'ťquation associťe s'ťcrit :
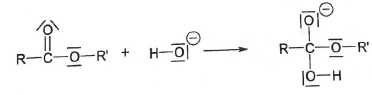
A. Il s'agit d'une ťtape correspondant ŗ une rťaction d'addition. Vrai.
B.
L'atome d'oxygŤne de l'ion hydroxyde est un site donneur de doublet d'ťlectrons ( site nuclťophile ). Vrai.
C. Dans la molťcule d'ester, le site nuclťophile mis en jeu est l'atome de carbone explicitement reprťsentť. Faux.
... le site ťlectrophile mis en jeu est l'atome de carbone explicitement reprťsentť.
D. Si le groupe R' se rťduit ŗ un atome d'hydrogŤne, cette ťtape est une rťaction acido-basique. Faux.
|
|
|
Exercice 5.
Le formiate d'ťthyle est un ester utilisť comme solvant pour dissoudre
le nitrate de cellulose, l'acťtate de cellulose et diffťrentes rťsines.
Il est ťgalement utilisť comme arŰme pour des saveurs fruitťes. On
donne la formule topologique du formiate d'ťthyle.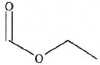
A. Cette molťcule possŤde le groupe caractťristique carbonyle. Faux, groupe ester.
B. Le formiate d'ťthyle se nomme le mťthanoate d'ťthyle en nomenclature officielle. Vrai.
C. La formule brute du formiate d'ťthyle est C3H5O2. Faux, C3H6O2.
D. Aucun des trois spectres RMN du proton ci-aprŤs ne peut Ítre celui du formiate d'ťthyle. Faux.
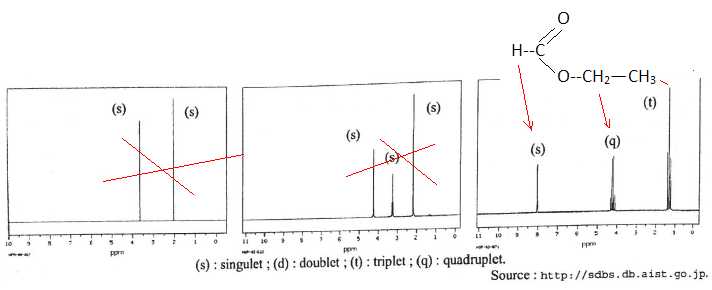
Exercice 6.
On ťtudie la transformation chimique modťlisťe par : :
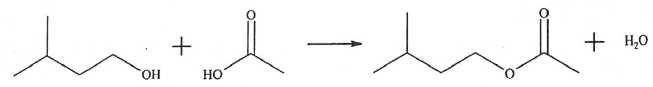
On
introduit 30 mL d'acide carboxylique liquide pur et 30 mL d'alcool
liquide pur. A l'issue de cette synthŤse on recueille, en plus de
l'eau, une masse m(ester) = 13 g d'ester liquide pur
M(alcool) =
88 g/mol ; M(acide) = 60 g/mol ; M(ester) = 130 g/mol ; densitť des
liquides : d(alcool) = 0,80 ; d(acide) = 1,0. Aide : 24 / 60 =0,40 ; 24
/ 881260,27 ; 30 / 88 ~0,34.
A. L'alcool utilisť est le 2-mťthylbutan-1-ol. Faux, 3-mťthylbutan-1-ol.
B. Le mťlange initial contien 0,27 mol d'alcool. Vrai.
m(alcool) =30 *0,80 = 24 g ; n(alcool) = 24 / 88 ~0,27 mol.
C. L'acide carboxylique a ťtť introduit en excŤs. Vrai.
m(acide) = 30 g ; n(acide) = 30 / 60 = 0,50 mol.
0,27 mol d'alcool rťagit avec 0,27 mol d'acide en donnant au mieux 0,27 mol d'ester.
D. Le rendement de cette synthŤse est 50%. Faux.
Quantitť de matiŤre rťelle d'ester : 13 /130 =0,10 mol
Rendement : 0,10 / 0,27 ~0,37 ( 37 %).
|
|
|
|
Exercice 7.
La
(S)-carvone est une espŤce chimique que l'on trouve en quantitť notable
dans l'aneth et les gaines de carvi, d'oý dťrive son nom. Elle est
susceptible de subir de nombreuses rťduction,notamment en carvomenthol
par hydrogťnťtion catalytique ŗ hautes tempťrature et pression et en
dihydrocarvone en prťsence de zinc dans l'acide ťthanoÔque.
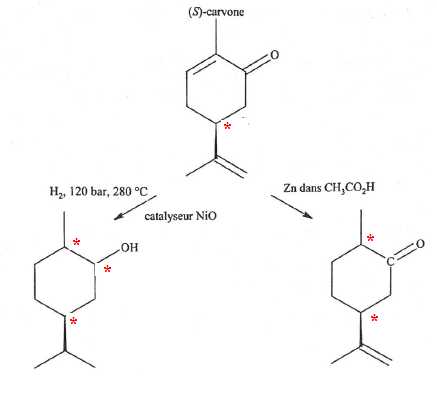
A. La (S)-carvone est une molťcule achirale. Faux.
B.
Pour chacune des rťactions de la (S)-carvone prťsenntťes ci-dessus, le
dihydrogŤne et le zinc sont des rťactis chimiosťlectifs. Faux.
Seul le zinc est chimiosťlectif, alors que le dihydrogŤne rťduit ŗ la fois les liaisons double C=C et le groupe carbonyle.
C. Le carvomenthol possŤde trois atomes de carbone asymťtriques. Vrai.
D. Dans la molťcule de dihydrocarvone, l'atome de carbone explicitement reprťsentť porte une charge partielle positive. Vrai.
Exercice 8.
L'ťquation de synthŤse de l'acťtate d'ťthyle est :
CH3COOH +C2H5OH = CH3-COO-CH2-CH3 + H2O.
On prťsente un protocole expťrimental.
Etape 1
: dans un ballon de 100 mL introduire un mťlange de 0,25 mol d'acide
acťtique et de 0,25 mol d'ťthanol. Y ajouter 0,50 mol d'acide
sulfurique concentrť et quelques grains de pierre ponce. Porter le
mťlange ŗ ťbullition ans un dispositif de chauffage ŗ reflux pendant 30
min.
Etape 2 :
laisser refroidir le mťlange ŗ l'air ambiant, puis dans un bain d'eau
froide. Verser le contenu du ballon dans une ampoule ŗ dťcanter
contenant 50 mL d'eau salťe. Agiter prudemment quelques instants en
dťgazant rťguliŤrement, puis ťliminer la phase aqueuse.
Etape 3
: ajouter ŗ la phase organique 60 mL d'une solution aqueuse de
dihydrogťnocarbonate de sodium ŗ 1,0 mol/L. Laisser dťgazer et
dťcanter, puis ťliminer la phase aqueuse. Recueillir la phase
organique, la sťcher sur chlorure de calcium anhydre puis filtrer.
Recuillir le filtrat dans un erlenmeyer propre et sec.
La synthŤse permet de recueillir 8,8 mL de filtrat.
A. Le montage de chaufage ŗ
reflux nťcessite l'utilisation d'une colonne ŗ distiller de Vigreux.
Faux. (rťfrigťrant ŗ eau ŗ boules).
B. L'acide sulfurique agit ici comme un facteur cinťtique. Vrai, rŰle de catalyseur.
C. Lors des ťtapes 2 et 3, la phase organique occupe la partie supťrieure de l'ampoule ŗ dťcanter. Vrai.
L'ester et l'ťthanol ont une densitť infťrieure ŗ celle de l'eau.
D. Le rendement de cette synthŤse est de 37 %. Faux.
Densitť : d(acide) =1,05 ; d(alcool) = 0,789 ; d(ester) =0,925.
M(acide) = 60 g/mol ; M(alcool) = 46 g/mol ; M(ester) = 88 g/mol.
Quantitť de matiŤre expťrimentale d'ester : 8,8 *0,925 / 88 = 0,0925 mol.
On peur espťrer obtenir au mieux 0,25 mol d'ester.
Rendement : 0,0925 / 0,25 = 0,0925*4 = 0,37 ( 37 %). Vrai.
Exercice 9.
Dans
un becher de 200 mL muni d'un barreau aimantť et placť sur un agitateur
magnťtique, on verse 75 mL d'un mťlange eau-ťthanol ŗ 50 % dans lequel
on introduit une cellule de conductimťtrie. A l'instant de date t=0, on
introduit 2,0 mL de 2-chloro-2-mťthylpropane pur dans le becher sous
vive agitation, puis on relŤve la conductance G du mťlange rťactionnel
au cours du temps. Les rťsultats expťrimentaux, obtenus ŗ une
temprťature de 20 įC sont prťsentťs sur le graphe ci-dessous.
L'ťquation de la rťaction associťe ŗ la transformation, supposťe
totale, s'ťcrit :
RCl aq + 2H2O---> ROH + H3O+aq + Cl-aq.
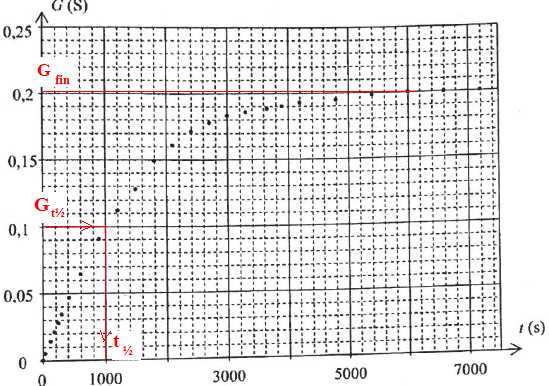
La conductance G, exprimťe en siemens (S), du mťlange rťactionnel est liťe ŗ la conductivitť s exprimťe en S m-1, par G = s
/ K oý K est la constante de cellule. On dťfinit, ŗ l'instant t, la
vitesse volumique de la rťaction par v(t) = BdG(t) / dt, oý B est une
constante.
A. Du point de vue des dimensions, K = l / S oý S et l sont respectivement la surface des ťlectrodes de la cellule et la distance qui les sťpare. Vrai. K s'exprime en m-1.
B. La vitesse volumique de cette rťaction commence par augmenter au cours du temps avant de s'annuler. Faux.
La pente de la tangente ŗ la courbe est maximale ŗ l'instant initial, puis diminue jusqu'ŗ s'annuler ( tangente horizontale).
C. En rťalisant une expťrience identique ŗ 40įC, le mťlange rťactionnel atteint la conductance maximale dans un dťlai plus court. Vrai.
D. Le temps de demi-rťaction est d'environ 3000 s. Faux.
Exercice 10.
On asimile le carburant automobile ŗ de l'octane de formule brute C8H18 qui brŻle dans l'air lorsqu'il est consommť pour alimenter le moteur du vťhicule. Densitť de l'octane d = 0,70.
A.
L'octane prťsente deux stťrťoisomŤres Z/E parmi tous ses isomŤres. Faux.
L'isomťrie de type Z/E ne concerne pas les alcanes.
B. L'ťquation de la rťaction de combustion complŤte de l'octane dans l'air s'ťcrit :
C8H18(l) + 25 O(g) --> 8CO2 (g) + 9H2O(g). Faux.
C8H18(l) + 12,5 O2(g) --> 8CO2 (g) + 9H2O(g).
C. Sous une pression donnťe, la tempťrature d'ťbullition de l'octane est supťrieure ŗ celle de l'heptane. Vrai.
F. Le vťhicule consomme 4,0 L de carburant aux 100 km. L'estimation des ťmissions de CO2 est lťgŤrment supťrieure ŗ 100 g km-1. Faux.
Pour 100 km : masse d'octane m(octane) = 4*0,70 = 2,8 kg
M(octane) =12*8 +18 =114 g/mol ; n(octane) = 2,8 103 / 114 =24,56 mol ;
n(CO2) = 8*24,56 ~196 mol.
M(CO2) = 44 g/mol ; m(CO2) = 44*196 ~ 8,6 103 g.aux 100 km soit ~ 86 g km-1.
|
|