QCM chimie.
Concours kinť Ceerrf 2016.
En poursuivant votre navigation sur ce site, vous acceptez l’utilisation de Cookies vous proposant des publicitťs adaptťes ŗ vos centres d’intťrÍts.
|
|
.
.
|
|
|
|
|
|
|
|
Question 1.
On
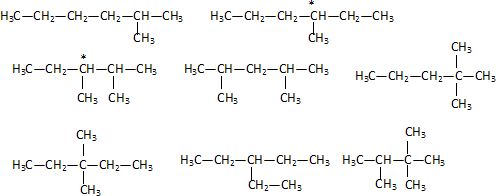
considŤre un hydrocarbure A non cyclique et saturť. A a pour masse
molaire M = 100 g/mol. A appartient a une famille de x isomŤres de
constitution ; x a pour valeur : 4, 5, 6, 7, 8, aucune valeur exacte.
CnH2n+2 ; M = 12n+2n+2 = 14 n+2 = 100 ; n =7.
CH3- CH2- CH2-CH2- CH2- CH2- CH3.
Question 2.
Lorsqu'on mťlange du 2-bromopropane avec des ions hydroxyde, il se
forme majoritairement un composť organique A de formule brute C3H8O. Pour identifier ce composť, des analyses spectrales ont ťtť rťalisťes.
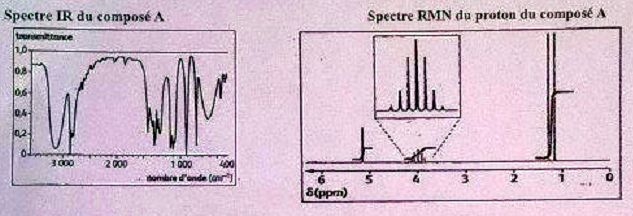
Choisir la ou les affirmation(s) correcte(s).
A. La formule topologique de A est 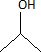 Vrai. Vrai.
Large bande vers 3300 cm-1, alcool associť par liaison hydrogŤne.
B. La formule topologique de A est : 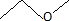 Faux. Faux.
C. La formule semi-dťveloppťe de A est : CH3-CH2-CH2-OH. Faux.
Le spectre RMN d'une telle molťcule prťsente 4 groupes de protons.
D. Il se forme ťgalement de l'eau au cours de la rťaction. Faux.
CH3-CHBr-CH3 + HO- ---> CH3-CHOH-CH3 + Cl-.
E. Il s'agit d'une rťaction d'ťlimination. Faux, substitution.
F. Aucune des 5 affirmations n'est exacte.
Question 3.
On considŤre une solution aqueuse d'un acide faible AH de concentration CA. Le pKa du couple AH / A- vaut 1,5. On rťalise le dosage d'un volume VA =10 mL de cet acide par une solution B de soude de concentration CB =0,10 molL. Le volume de soude versť ŗ l'ťquivalence est VE = 1,0 mL
Choisir la ou les affirmation(s) correcte(s).
A. A l'ťquivalence de ce dosage le pH est supťrieur ŗ 7. Vrai.
La solution contient majoritairement la base faible A-.
B. A l'ťquivalence de ce dosage le pH est infťrieur ŗ 7. Faux.
C. CA = 1,0 10-3 mol/L. Faux.
CA = CB VE / VA = 0,10 *1,0 / 10 = 0,010 mol/L.
D. CA = 1,0 10-1 mol/L. Faux.
E. Le pH de la demi-ťquivalence est ťgal ŗ pKa = 1,5. Vrai.
F. Aucune des 5 affirmations n'est exacte.
Question 4.
On donne les formules des principes actifs de trois mťdicaments.
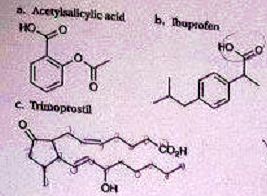
Choisir la ou les affirmation(s) correcte(s).
A. Une seule molťcule parmi les trois possŤde le groupe carboxyle. Faux.
B. Les trois groupes OH visibles sur les molťcules prťsentťes correspondent ŗ des fonctions alcools. Faux.
OH du groupe alcool et du groupe carboxyle.
C. Les trois molťcules possŤdent au moins trois doubles liaisons conjuguťes. Faux.
D. La formule brute du trimoprostil est C22H33O4. Faux. C21H34O4.
E. La molťcule d'acide salicylique prťsente un groupe carbonyle. Faux.
Groupe carboxyle et groupe ester.
F. Aucune des 5 affirmations n'est exacte. Vrai.
|
|
|
Question 5.
Le sel de Mohr est un solide de formule FeSO4, (NH4)2SO4, 6H2O.
On dissout du sel de Mohr dans un volume V = 500 mL d'eau afin
d'obtenir une solution dont la concentration en sel de Mohr est c =
2,00 10-2 mol/L.
A. Le sel de Mohr est un solide molťculaire neutre. Faux, solide cristallin.
B. Pour prťparer la solution il faut peser m = 15,6 g de sel de Mohr. Faux.
M( sel de Mohr) = 55,8 +2*32,1+14*16+2*14+20=392 g/mol.
n = cV = 0,0200 *0,500 = 0,0100 mol ; m = 392*0,0100 =3,92 g.
C. Pour prťparer la solution il faut peser m = 3,95 g de sel de Mohr. Faux.
D.
Le prťcipitť d'hydroxyde de fer obtenu par ajout de quelques
gouttes d'une solution d'hydroxyde de sodium ŗ un prťlŤvement de
la solution a pour formule Fe(OH)2 (s). Vrai.
D. Dans la solution, la relation entre les concentrations molaires des ions NH4+ et SO42- vťrifie [NH4+]=[SO42-]=0,5 c. Faux. [NH4+]=[SO42-]=2 c.
F. Aucune des 5 affirmations n'est exacte. Faux.
Question 6.
L'ťnergie thermique fournie par un bec Bunsen, alimentť en propane, est
rťglťe ŗ 4000 kJ /h. L'ťnergie transfťrťe au cours de la combustion
complŤte d'une mole de propane est en valeur absolue Qr = 2,00 103 kJ /mol. On donne Vm
= 25 L/mol; L'air est constituť de 20% de dioxygŤne en volume. Le dťbit
volumique de l'air admis par la virole ( entrťe d'air) du bec Bunsen
est ( m3 h-1) : 1,39 ; 3,00 ; 1,25 ( vrai) ; 1,50 ; autre. :
C3H8 +5O2 --> 3CO2 + 4H2O.
n(propane) = 4000 / 2000 = 2 mol / h. ; n(dioxygŤne) = 10 mol / h ; n(air) =50 mol /h.
Dťbit : 50*25 =1250 L / h = 1,25 m3 / h.
|
|
|
|
Question 7.
On considŤre une solution d'hydroxyde de calcium Ca(OH)2 obtenue par dissolution totale du solide ionique Ca(OH)2. Cette solution est telle que la concentration en ion calcium est ťgale ŗ 5,00 10-3 mol/L. Quel est le pH ŗ 25įC de cette solution ?
10,0 ; 11,0 ; 11,7 ; 12,0 vrai ; 12,4 ; autre.
[HO-] = 2 [Ca2+] = 1,00 10-2 mol/L.
pH = 14 + log ( 1,00 10-2) = 12,0.
C. Dans une formule mathťmatique, telle que exp(u), ln (u) ou cos (u),
u doit Ítre sans dimension. Vrai.
D. Dans une relation du type x y + z2 = t2, on
peut dire que z et t ont la mÍme dimension. Vrai.
E. Dans une relation
du type x y + z2 = t2, on peut dire que y a la
mÍme dimension que t. Faux.
Question 8.
Lorsqu'on met en prťsence du 2-bromopropane avec des ions hydroxydes HO-, l'un des produits qui se forme ŗ l'ťtat de traces a comme formule C3H6. Choisir la ou les affirmation(s) correctes.
A. C'est une rťaction de substitution. Faux. ( Ellimination).
CH3-CHBrCH3 + HO- --> CH3-CH=CH2 +H2O +Br-.
B. C'est une rťaction d'addition. Faux.
C. C'est une rťaction par transfert de doublet d'ťlectrons de l'atome d'oxygŤne de l'ion HO- vers l'atome de brome du 2-bromopropane. Faux.
D. Il se forme ťgalement du dibrome et de l'eau au cours de la rťaction. Faux.
E. L'une des liaison C-H du 2-dibromopropane est rompue. Vrai.
F. Aucune des affirmations prťcťdentes n'est correcte. Faux.
Exercice 9.
A propos des isomŤres de constitution du butanol ( appartenant ŗ la mÍme famille que ceui-ci). Choisir la ou les affirmation(s) correctes.
A. L'un des isomŤres prťsente un spectre RMN avc uniquement deux signaux : deux singulets. Vrai.
(CH3)3C-OH.
B. L'un des isomŤres prťsente un spectre RMN contenant un heptuplet. Faux.
C. Les spectres RMN des isomŤres prťsentent tous un doublet. Faux.
D. Deux des isomŤres sont des alcools secondaires. Faux.
CH3-CH2-CH2-CH2OH et (CH3)2CH-CH2OH ( alcools primaires) ;
CH3-CH2-CHOH-CH3.( alcool secondaire) ; (CH3)3C-OH. ( alcool tertiaire ).
E. On peut les distinguer par spectroscopie IR sans tenir compte de la partie " empreinte du spectre".. Faux.
F. Aucune des affirmations prťcťdentes n'est correcte. Faux.
Exercice 10.
Le propan-2-ol est lentementoxydť par les ions permanganate pour former C3H6O.
A une date t=0, ŗ la tempťrature de 30įC, on introduit dans un
erlenmeyer 1,0 mL de propan-2-ol et 50 mL d'une solution de
permanganate de potassium acidifiť de concentration c0 =
0,20 mol/L. On suit lťvolution temporelle de la transformation en
dťterminant pťriodiquement l'avancement de la rťaction. On prťlŤve ŗ
une date t, un volume du mťlange rťactionnel auquel on ajoute de l'eau
glacťe. Par dosage, on dťtermine la concentration des ions MnO4-
contenus dans le prťlŤvement, pour dťterminer l'avancement x. On
renouvelle l'opťration ŗ diffťrentes dates t on obtient la courbe (a)
ci-dessous.
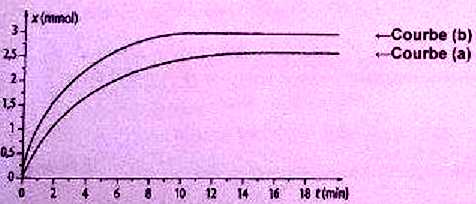
On donne : masse volumique du propan-2-ol : r =0,80 g/L ; M(C3H8O) = 60 g/mol ; couples redox C3H6O / C3H8O ; MnO4- / Mn2+ ; seul MnO4- est colorť ( violet). Choisir la ou les affirmation(s) correctes.
A. L'ion permanganate a ťtť introduit en dťfaut. Faux.
5C3H8O + 2MnO4- +6H+ -->2 Mn2+ +5C3H6O +8H2O.
n(C3H8O) =0,80 / 60=0,0133 mol ; n(MnO4-) =0,050*0,20 =0,01 mol.
0,0133 mol d'alcool rťagit avec 0,0133 / 2,5 =0,0053 mol d'ion permanganate.
B. Cette rťaction peut Ítre suivie par spectroscopie en rťglant le spectrophotomŤtre sur une longueur d'onde de 420 nm. Faux.
La
solution ťtant violette elle prťsente un maximum d'absorption dans le
rouge. Il faut choisir une longueur d'onde correspondant ŗ ce maximum.
C. L'ajout d'eau glacťe a pour seul but de diluer le mťlange. Faux, blocage cinťtique.
D. A 30įC, le temps de demi-rťaction est de 7 minutes. Faux ( ~ 2 minutes).
E. La courbe (b) a ťtť obtenue aprŤs ajout d'un catalyseur dans le milieu rťactionnel. Faux.
Un catalyseur accťlŤre la rťaction sans modifier la composition finale.
F. Aucune des affirmations prťcťdentes n'est correcte. Vrai.
|
|