Les bulles du
champagne.
Concours général SPCL 2016.
En poursuivant votre navigation sur ce site, vous acceptez l’utilisation de Cookies vous proposant des publicités adaptées à vos centres d’intérêts.
|
|
.
.
|
|
|
|
|
|
|
|
Le service d'une flûte.
Le
champagne est généralement servi dans une flûte que l'on garde
verticale au cours du service. Ce service diffère de celui de la bière
que l'on verse en inclinant le verre. La concentration en CO2 dissout dans le champagne après service a été mesurée pour les deux types de service et pour différentes températures.
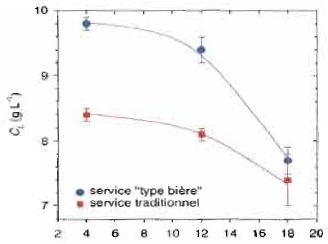
39. Argumenter brièvement l'avantage d'incliner le verre pour servir le champagne.
A température inférieure à12°C, ce type de service conserve beaucoup plus de CO2 dissout dans le champagne, donc davantage de bulles.
La nucléation et la montée des bulles dans le champagne.
Les bulles se forment ( ou nucléent ) au niveau des irrégularités ou
impuretés sur la surface interne du verre. le dioxyde de carbone
dissout dans le champagne est alors transformé en gaz carbonique. On
peut alors observer au-dessus d'un site de nucléation un "train de
bulles".

|
La barre verticale noire mesure 1mm.
40. Commenter la photographie ci-contre.
On observe deux phases dans la montée :
au début le mouvement est uniformément accéléré, puis le mouvement est
rectiligne uniforme. Le diamètre des bulles augmente au cours de la
montée.
On s'intéresse au mouvement ascendant d'une bulle de champagne d'un diamètre initial de 2,0 10-4 m dans une flûte. On suppose que la masse et le volume de la bulle reste constant au cours du mouvement.
41. Calculer la masse de la bulle à 12°C à la pression atmosphérique, sachant que la densité du gaz carbonique est 1,9 kg m-3 à cette température.
Volume de la bulle : V = 4 /3 pr3 = 4/3*3,14 (10-4)3=4,186 10-12 m3.
Masse d'une bulle m = 4,186 10-12 *1,9 =7,955 10-12 ~8,0 10-12 kg.
En plus de la force de pesanteur, la bulle est soumise à une force de
la part du liquide, la poussée d'Archimède verticale, dirigée vers le
haut, de norme Vrg où r est la masse volumique du liquide.
42. Schématiser une bulle et les forces auxquelles elle est soumise.
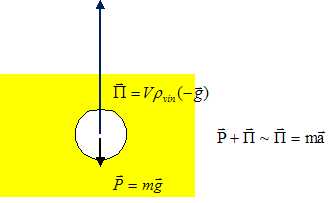
43. Comparer le poids de la bulle et la poussée d'Archimède. Conclure.
P = mg = 8,0 10-12 *9,81 ~7,8 10-11N.
P = V rvin g =4,186 10-12 *1000 *9,81 ~ 4,1 10-8 N.
Le poids est négligeable devant la poussée.
|
44. En déduire la nature du mouvement de la bulle juste après sa formation.
Mouvement rectiligne uniformément accéléré vers le haut.
En
réalité, il convient de prendre en considération la résistance du
fluide lors de l'ascension de la bulle. On suppose que la bulle est
soumise à une force de frottement visqueux de la part du fluide, de
sens opposé au mouvement, dont l'expression est : f = 4 p hR v où h est la viscosité dynamique du champagne ( 1,0 10-3 Pa s), R le rayon de la bulle et v sa vitesse. Après un temps très court, la bulle atteint une vitesse constante.
45. Représenter l'allure d'une chronographie de la montée de la bulle.
46. Schématiser l'évolution des forces au cours du mouvement.
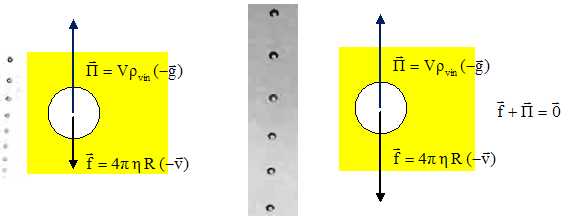
47. Déterminer la valeur de la vitesse atteinte par la bulle.
V rvin g = 4 p h R v ; v = V rvin g / ( 4 p h R ).
v = 4,186 10-12 *1000*9,81 /(4*3,14*10-3* 10-4)=3,27 10-2 ~3,3 10-2 m / s.
48.
Estimer la durée nécessaire à une bulle pour remonter à la surface
d'une flûte remplie de champagne jusqu'à une hauteur de 12 cm. Cette
durée vous paraît-elle pertinente ?
0,12 / (3,27 10-2)~3,7 s. Cette durée paraît faible par rapport à la réalité.
49. Au vu de la photographie du train de bulles, commenter l'hypothèse faîte à la qustion 40.
Le volume des bulles n'est pas constant au cours de la montée.
50. En ralité, au cours de la montée de la bulle, la masse et le volume de la bulle augmentent : du CO2
dissout continue à passer en phase gaseuse dans la bulle tout au long
de l'ascension de la bulle. Expliquer qualitativment l'influence de
cette croissance de la bulle sur sa vitesse de montée.
Le poids de la bulle reste négligeable devant la poussée. Si le volume de la bulle augmente, la vitesse de remontée croît.
|
|
|
L'explosion des bulles de champagne en surface.
Lorsque
le champagne est servi dans un verre,les bulles arrivant à la surface
éclatent et génèrent des gouttelettes montant au dessus de la surface
du champagne. L'aérosol ainsi généré est reconu pour ses propriétés
organoleptiques ( c'est à dire agissant sur la perception
sensortielle). Des chercheurs ont cherché à révéler si les compositions
du champagne et de cet aérosol étaient différentes. On trouve dans les
aérosols des acides gras qui sont présents, mais de façon très dilués
dans le champagne.
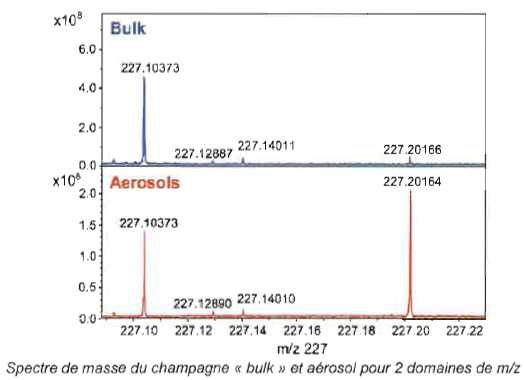
Un
acide gras saturé est un acide carboxylique aliphatique comportant de
12 à 24 atomes de carbone et aucune double liaison cabone-carbone. La
formule semi-développée d'un tel acide gras à n atomes de carbone étant
H3C(-CH2)n-2-COOH.
Un acide gras insaturé est un acide gras qui comporte une ou plusieurs doubles liaisons carbone carbone.
51. Donner la formule semi-développée de l'acide dodécanoïque ( ou acide laurique) et de l'ion dodécanoate.
H3C(-CH2)10-COOH ;
H3C(-CH2)10-COO-.
|
|
|
|
52.
Ecrire la formule brute d'un ion carboxylate saturé ( en fonction de n,
nombre d'atomes de carbone ) et d'un ion carboxylate monoinsaturé.
Saturé : H3C(-CH2)n-2-COO- soit Cn H2n-1O2-.
Monoinsaturé : Cn H2n-3O2-.
53. Exprimer la masse molaire d'un ion carboxylate saturé en fonction de n et d'un ion carboxylate monoinsaturé.
Saturé : M = 12 n +2n-1 +2*16 = 14 n+31 g/mol.
Monoinsaturé : M = 12 n +2n-3 +2*16 = 14 n+29 g/mol.
54. Proposer une stratégie expérimentale pour récupérer uniquement le liquide contenu dans l'aérosol.
Tenir
la flûte de champagne suffisament inclinée pour que le liquide reste
dans la flûte et que l'aérosol tombe dans un récipient assez large
situé sur la table en dessous de la flûte.
55.
Identifier les deux ions carboxylates ( obtenus après ionisation )
présents en excès dans l'échantillon aérosol ( aucun n'est polyinsaturé
). En déduire les formules brutes des deux acides carboxyliques
présents en excès dans l'aérosol.
m/z = 227 :
Hypothèse : ion carboxylate saturé 227 = 14n +31 ; n =14.
n est entier, l'hypothèse est valide. C14 H27O2- et C14 H28O2 .
m/z = 253 :
Hypothèse : ion carboxylate saturé 253 = 14n +31 ; n =15,8.
n n'est pas entier, l'hypothèse n'est pas valide.
Hypothèse : ion carboxylate monosaturé 253 = 14n +29 ; n =16.
n est entier, l'hypothèse est valide. C16 H29O2- et C16 H30O2 .
56.
Expliquer, grâce à un schéma, que les acides carboxyliques ont un
caractère amphiphile, c'est à dire qu'ils présentent à la fois un pôle
hydrophile et un pôle hydrophobe.
Le groupe carboxyle COOH, polaire,
est ami de l'eau ( caractère hydrophile ), solvant polaire ; la longue
chaine carbonée est ennemie de l'eau, caractère hydrophobe. Une molécule de tensioactif est
représentée comme ci-dessous :
---------------------O
Queue hydrophobe .... tête
hydrophile.
57. Expliquer pourquoi les acides gras sont particulièrement présents dans les gouttelettes d'aérosol de champagne.
Les bulles de champagne sont constituées
de dioxyde de carbone gazeux.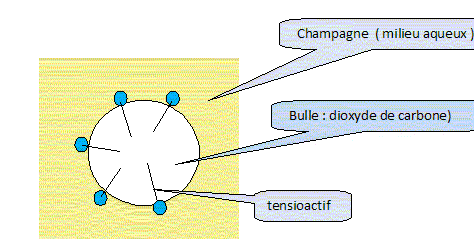
|
|
|
|