Synthèse de la
phénylalanine.
BTS Bioanalyses et controles 2016.
En poursuivant votre navigation sur ce site, vous acceptez l’utilisation de Cookies vous proposant des publicités adaptées à vos centres d’intérêts.
|
|
.
.
|
|
|
|
|
|
|
|
1.1. Entourer et nommer les deux fonctions chimiques présentes dans cette molécule.
1.2. Repérer, par un astérisque, l'atome de carbone asymétrique.
1.3. Cette molécule est chirale. Préciser ce que cela signifie ?
Fonctions amine et acide carboxylique.
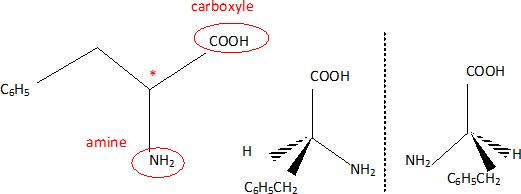 Une molécule chirale (
présence d'un carbone asymétrique, dans ce cas ) existe sous la forme
de deux énantiomères non superposables, image l'un de l'autre dans un
miroir plan.
Une molécule chirale (
présence d'un carbone asymétrique, dans ce cas ) existe sous la forme
de deux énantiomères non superposables, image l'un de l'autre dans un
miroir plan.
La synthèse s'effectue en plusieurs étapes à partir du benzène.
1ère étape. On fait réagir du chlorométhane CH3-Cl sur le benzène en présence de catalyseur. On obtient le composé A.
2.1. Ecrire l'équation de la réaction.
C6H6 + CH3-Cl --> C6H5-CH3 + HCl.
2.2. Donner le nom d'un catalyseur couramment utilisé pour cette réaction.
Trichlorure d'aluminium AlCl3.
2ème étape. A réagit avec le dibrome, en présence de lumière, pour conduire à B.
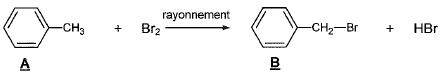
3.1. Parmi les termes suivants, choisir celui ( ceux) qui caractérise(nt) la transformation.
addition, électrophile, élimination, nucléophile, radicalaire, substitution.
Proposer un type de rayonnement adapté.
Substitution radicalaire en présence de lumière UV.
|
|
|
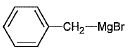
3ème étape. L'action du magnésium sur B dans l'éther anhydre donne le composé C.
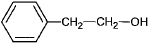
4ème étape. Le composé C réagit avec le méthanal pour donner, après hydrolyse en milieu acide, l'alcool D.
4.1 Préciser la famille chimique du composé C.
C est un organomagnésien.
4.2. Ecrire la formule semi-développée du méthanal.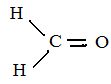
4.3. Le groupe
carbonyle du méthanal subit une addition nucléophile. Préciser la
particularitéé du groupe carbonyle C=O qui permet d'expliquer cette
addition.
L'atome d'oxygène est plus électronégatif que l'atome de carbone. La
liaison est polarisée. L'atome de carbone est déficitaire en électrons.
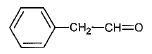
4.4. Nommer l'alcool D.
2-phényléthanol.
|
|
|
|
5ème étape. L'alcool D oxydé par les ion permanganate MnO4- en milieu acide, conduit à l'aldehyde E.
5.1. Ecrire les demi-équations électroniques mises en jeu.
5.2. En déduire l'équation de la réaction.
5 fois { C6H5CH2CH2OH = 2H+ + 2e- + C6H5CH2CHO }
2 fois { MnO4- + 8H+ + 5e- = Mn2+ + 4 H2O }
5 C6H5CH2CH2OH + 2 MnO4- + 6H+ = 5 C6H5CH2CHO + 2 Mn2+ + 8 H2O .
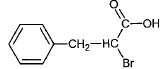
6. D'autres étapes, non
étudiées ici, permettent d'obtenir le composé H à partir du composé E.
Finalement l'action de l'ammoniac NH3 sur H donne la phénylalanine.
6.1. Ecrire la formule de Lewis de la molécule d'ammoniac.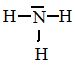
6.2 En déduire la propriété de l'ammoniac mise en jeu dans cette réaction.
L'ammoniac est nucléophile il pourra réagir avec le carbone électrophile porteur du brome.
|
|