Séparation d'acide
a-aminés par
électrophorèse. Bac S Nlle Calédonie 03/2016.
En poursuivant votre navigation sur ce site, vous acceptez l’utilisation de Cookies vous proposant des publicités adaptées à vos centres d’intérêts.
|
|
|
|
|
|
|
|
On s'intéresse au principe de la séparation des protéines par électrophorèse.
La
technique consiste à séparer les constituants d'un mélange de protéines
déposé sur un support horizontal ( papier à acétate, gel d'amidon, ..)
en le soumettant à un champ électrique uniforme E. La séparation repose
essentiellement sur les différences de charge électrique et de taille
des constituants du mélange.
Les constituants sont supposés immobiles avant que la tension ne soit appliquée.
Quelques fractions de secondes après le début de l'application du champ
électrique, pour chaque constituant du mélange, la force de frottement
f, de module f = kRv, compense la force électrique avec :
k : constante positive caractéristique du constituant et du milieu où s'effectue la migration ;
R : rayon de Stockes du constituant. Ce rayon est d'autant plus grand que le constituant est plus volumineux ;
v : vitesse du constituant.
1. Migration des constituants lors de l'électrophorèse.
1.1 Justifier que le mouvement de migration des constituants est rectiligne uniforme.
Le poids d'un constituant est compensé par l'action du support.
Quelques
fractions de secondes après le début de l'application du champ
électrique, pour chaque constituant du mélange, la force de frottement
f, de module f = kRv, compense la force électrique.
D'après le principe d'inertie, le centre d'inertie d'un solide pseudo-isolé est animé d'un mouvement rectiligne uniforme.
1.2 Montrer que la vitesse de migration d'un constituant est v = |q|E / (kR).
Valeur de la force électrique exercée sur une espèce de charge q : F = |q| E.
Valeur de la force de frottement : f = k R v.
Ces deux forces ont même module : |q| E =k R v ; v =|q|E / (kR).
1.3. Tous les constituant se déplace t-il à la même vitesse ? Justifier.
Pour
un champ E et un support donnés, la vitesse dépend de la valeur absolue
de la charge et de la taille des constituants. Les constituants n'ont
pas tous la même vitesse.
On choisit une durée de 40 min pour réaliser l'électrophorèse. Pour un constituant tel que kR = 2,2 10-12 N s m-1 et portant une charge élémentaire q = 1,6 10-19 C, placée dans un champ électrique E = 7,5 102 V m-1 :
1.4. Calculer la durée nécessaire pour obtenir une mgration de 10 cm. Conclure sur la durée choisie initialement.
v = 1,6 10-19 *7,5 102 / (2,2 10-12) =5,45 10-5 m/s.
Durée nécessaire pour parcourir 10 cm : 0,10 / (5,45 10-5) =1,83 103 s~31 min.
La durée de 40 min est correctement choisie.
|
|
|
2. Séparation d'un mélange d'acide a-aminés.
On modélise un mélange noté M de protéines par une solution aqueuse de suatre acide a-aminés : la lysine, la glycine, l'acide aspartique et l'acide glutamique.
A
partir des documents ci-après, représenter les domaines de prédominance
des quatre acides aminés évoqués ci-dessus. A partir des réponses aux
questions précédentes et des connaissances acquises, associer à chaque
tache obtenue lors de l'électrophorèse du mélange M, l'acide a-aminé qui lui correspond.
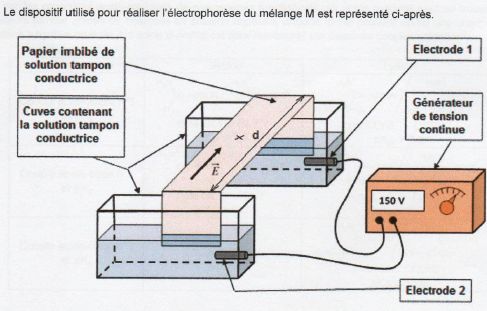
Le support de migration est une feuille de papier de type acétate de
cellulose. Celui-ci est imprégné d'une solution tampon de pH = 6,0.
Quelques gouttes du mélange M sont déposées au centre de la feuille marquées d'une croix.
Le
générateur de tension, réglé sur la tension U = 150 V est mis en
fonctionnement pendant plusieurs heures. Il produit le champ électrique
E, supposé uniforme, dont la direction et le sens sont indiqués.
Le générateur est éteint puis on vaporise sur la feuille, sous hotte, du réactif à la ninhydrine, lequel colore les acides a-aminés afin de rendre visible leur position sur le papier après migration.
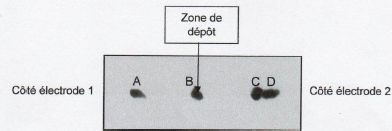
La feuille de papier laisse apparaître 4 taches, notées A, B, C et D.
Les taches C et D sont seulement légèrement séparées. Chaque tache
correspond à l'un des acides a-aminés du mélange.
|
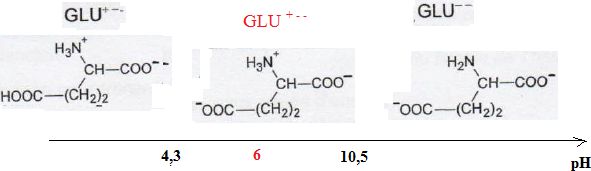
A pH = 6 la forme majoritaire de l' acide glutamique possède une charge globale négative, elle se déplace en sens contraire du champ.
Taches C ou D.
L'acide glutamique est plus volumineux que l'acide aspartique. L'acide glutamique se déplace moins vite que l'acide aspartique.
Acide glutamique : tache C ; acide aspartique : tache D.
|
|