Synthèse
asymétrique du menthol.
Bac S Asie 2016.
En poursuivant votre navigation sur ce site, vous acceptez l’utilisation de Cookies vous proposant des publicités adaptées à vos centres d’intérêts.
|
|
|
|
|
|
|
|
1.
Synthèse du (-) menthol par le procédé au thymol.
1.1. Donner les formules
semi-développées et topologique du propène.
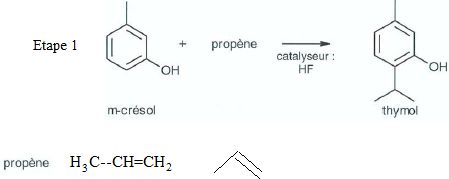
1.2. Choisir, en
justifiant, le type de réaction auquel appartient la réaction
d'hydrogénation du thymol
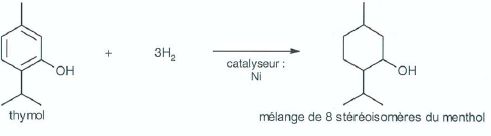
Addition du dihydrogène sur le thymol. A partir de deux réactifs, on
obtient un seul produit.
1.3. Indiquer par
des astérisques les atomes de carbone asymétriques du (-)menthol.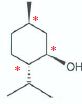
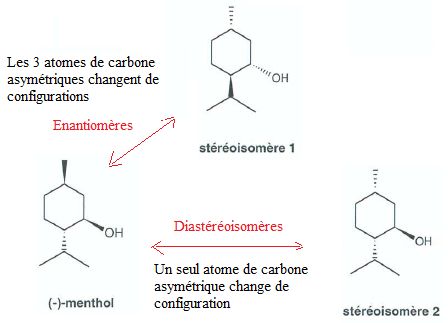
1.4 Deux
stéréoisomères du (-) menthol sont représentés ci_dessous. Préciser le
type d'isomérie qui lie le (-)menthol avec le stéréoiomère 1 d'une part
et avec le stéréoisomère 2 d'autre part. Justifier.
1.5 Si les deux étapes sont totales et si les 8 stéréoisomères du menthol sont obtenus dans les mêmes proportions, quel est le rendement de la synthèse du(-)menthol ?
1 /8 ~0,13 ( 13 %).
|
|
|
2. Synthèse du(-)menthol par le procédé Takasago..
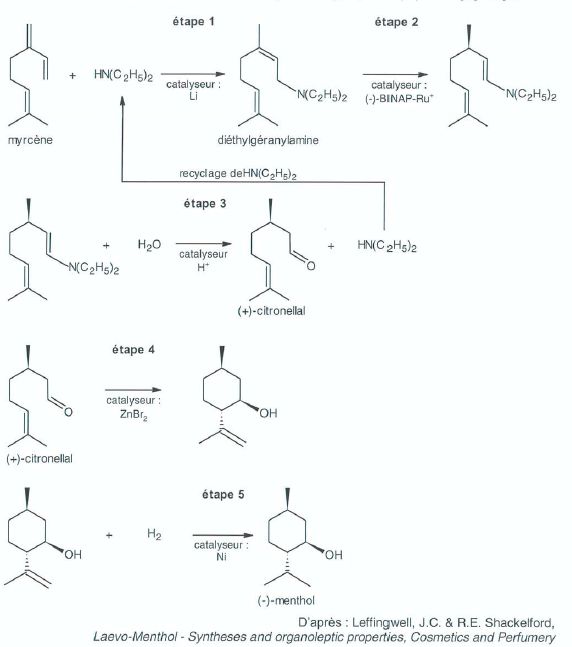
|
|
|
|
2.1. le myrcène présente-t-il une isomérie de type Z /E ? Justifier.
Les atomes de carbone doublement liés, situés en bout de chaine, portent des atomes ou groupes d'atomes identiques >C=CH2 ou >C=C(CH3)2 .
Le myrcène ne présente pas d'isomérie de type Z / E.
2.2.
Identifier les étapes créant un ou plusieurs atomes de carbone
asymétriques et indiquer celle impliquant une catalyse asymétrique.
L'étape n°2 créé un atome de carbone asymétrique ; l'étape n°4 créé deux atomes de carbone asymétriques.
L'étape n°2 utilise un catalyseur chiral : cette catalyse est asymétrique.
2.3 Compte tenu du recyclage de la diéthylamine, le bilan global du procédé peut s'écrire :
myrcène + X + Y --> (-)menthol.
Donner les formules brutes des deux molécules X et Y.
H2O et H2.
3. Comparaison des deux procédés de synthèse.
Présenter les points positifs du procédé Takasago par rapport au
procédé au thymol dans une perspective du respect des deux principes de
la chimie verte fournis.
Principe 9
: le procédé Takasago utilise des catalyseurs sélectifs alors que le
procédé au thymol met en oeuvre des catalyseurs non sélectifs.
Principe 2 : économie d'atomes.
Utilisation atomique : UA = M(produit recherché) / somme des masses molaires des réactifs ou somme des masse molaires des produits.
Procédé au thymol : UA = 1/8 = 0,125 après séparation des isomères.
Procédé Takasago: UA = 1 ( réaction sans sous-produit ).
Tous les atomes entrant dans le processus se retrouvent dans le produit final.
|
|