QCM : chimie
organique, cinétique chimique.
Concours kiné Rennes 2013
En poursuivant votre navigation sur ce site, vous acceptez l’utilisation de Cookies vous proposant des publicités adaptées à vos centres d’intérêts.
|
|
.
|
|
|
|
|
|
|
PUne molécule est constituée de trois
atomes de carbone dont l'un porte à la fois un groupe amine et un
groupe carboxyle.
A- Sa formule brute
est C3H8O2. ( faux ).
C3H7O2N.
B. Son nom en
nomenclature officielle est acide 2-aminopropanoïque. ( vrai
).
C- Cette molécule
peut posséder un caractère acide et un caractère basique. ( vrai ).
D-
Cette molécule est chirale. ( vrai).
Le carbone n°2 est
asymétrique CH3-CH NH2-COOH.
E- Les 4
affirmations précédentes sont fausses. ( faux ).
A-
Sa formule semi développée est NH2-CH2-CH2-COOH.
( faux ).
Le groupe amine et le
groupe carboxyle doivent être portés par le même carbone.
B. Dand l'acide
conjugué de la fonction amine, on a le groupe >CH-NH3+.
( vrai
).
C- La formule
développée peut correspondre à deux énantiomères Z et E. ( faux ).
D-
La formule topologique est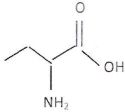 . ( faux). . ( faux).
Dans cette formule on
compte 4 atomes de carbone
E- Les 4
affirmations précédentes sont fausses. ( faux ).
Cette molécule est caractérisée par 2 pKa : pKa1
= 2,3 et pKa2 = 9,9.
A-
A pH inférieur à 9, le groupe amine est de façon prédominante sous la
forme -NH2. ( faux ).
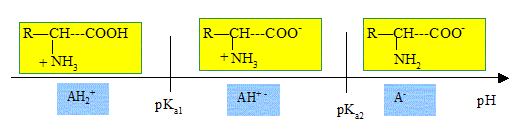 . .
B. A pH inférieur à
2, on a de façon prédominante -COO-. ( faux ).
C- A pH neutre, les deux groupes
fonctionnels sont sous les formes. -NH3+ et COO-
( vrai ).
D-
La molécule décrite ne présente jamais la forme prédominante en
solution aqueuse. ( faux).
E- Les 4
affirmations précédentes sont fausses. ( faux ).
|
| .
. |
|
|
On donne les spectres IR et RMN du proton d'une molécule organique
formée d'atome de carbone, d'hydrogène et de deux atomes d'oxygène.
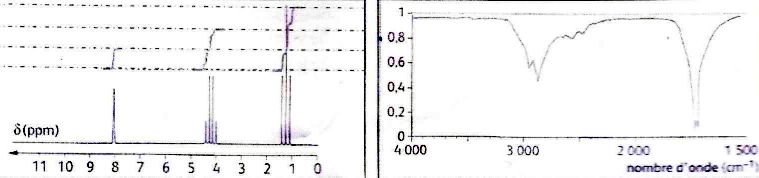
A-
Le spectre de gauche correspond au spectre IR. ( faux ).
B. Dans le specre de gauche, d signifie " écart relatif ".
( faux ).
déplacement chimique.
C- C'est
l'absorbance qui est mesurée en ordonnée sur le spectre de gauche. (
faux ) .
Transmitance en pourcentage.
D- Le nombre d'onde
3000 cm-1 correspond à une longueur d'onde dans le vide de
333 nm. ( faux).
1/3000 =3,33 10-4 cm
= 3,33 10-6
m = 3,33 µm.
E- Les 4
affirmations précédentes sont fausses. ( vrai ).
|
.
|
|
A- La formule brute la plus simple correspondant à ces spectres
est C3H6O2. ( vrai ).
La
courbe d'intégration ( spectre RMN ) indique 6 protons : ce qui correspond à 3 atomes de carbone et une
liaison double.
B.
Il existe une molécule chirale de formule brute C3H6O2.
( vrai ).
CH3- CH OH- CHO.
C- Il existe un
acide carboxylique de formule brute C3H6O2.
( vrai ).
CH3-CH2-COOH.
D- La formule
topologique suivante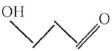 correspond à la formule brute C3H6O2.
( vrai ). correspond à la formule brute C3H6O2.
( vrai ).
E- Les 4
affirmations précédentes sont fausses. ( faux ).
A-
Le spectre RMN du proton montre
qu'il ne s'agit pas d'un acide carboxylique. ( faux ).
Le signal du proton du
groupe carboxyle peut être vers 8 ppm ; le spectre IR montrerait une
large bande entre 3000 et 3500 cm-1 dans le cas d'un acide
carboxylique .
B. Les deux spectres peuvent
correspondre à un ester. ( vrai
).
HCOO-CH2-CH3,
formiate d'éthyle.
C- Le triplet à 1,3
ppm du spectre RMN correspond à des protons portés par un atome de
carbone lié à un élément plus électronégatif car son déplacement est
faible. ( faux ) .
D-
La molécule étudiée est l'éthanoate de méthyle. ( faux).
Le
spectre RMN indiquerait 2 singulets correspondant à 2 groupes méthyle.
Il s'agit plutôt de HCOO-CH2-CH3.
E- Les 4
affirmations précédentes sont fausses. ( faux ).
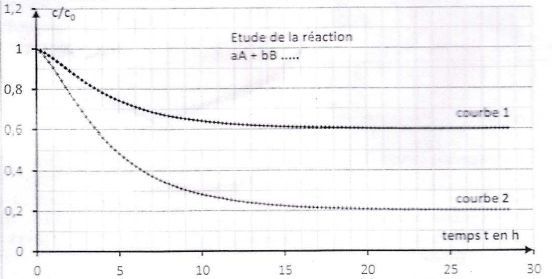
On considère une réaction chimique entre deux réactifs en solution
aqueuse A et B. La première partie de l'équation de cette réaction peut
s'écrire aA + bB où a et b sont des nombres stoechiométriques
inférieurs à 5. Pour étudier cette réaction, on trace en fonction du
temps et pour chaque réactif le rapport de sa concentration c à la date
t à sa concentration c0 à t=0, lors de la réalisation du
mélange. On dispose de solutions de A et B à la même concentration en
soluté apporté. A l'instant t=0, on mélange un volume V1 de
A et un volume V2 = 4 V1 de B.
A-
Au temps t=0, la concentration c0(A)
est égale à 1/5 de c0(B). ( faux ).
c0(A) = c0 V1
/(V1+V2) = c0 V1 /(V1+4V1)
=
c0/5 ; c0(B) = c0 V2 /(V1+V2)
= c0 4V1 /(V1+4V1)
=
4c0/5
.
B. Au temps t½, 50 % d'un
des réactifs a disparu. ( faux ).
A temps de demi-réaction
,l'avancement est égal à la moitié de l'avancement final. Or la
réaction est limitée, l'avancement final n'est pas égal à 1.
C- La réaction
aboutit à un équilibre chimique. ( vrai
).
c/c0, à la fin, n'est pas égal
à zéro.
D- La réaction est
rapide. ( faux).
L'état
final est atteint au bout de plusieurs heures.
E- Les 4
affirmations précédentes sont fausses. ( faux ).
|
|
|
A-
Le temps de demi-réaction est
compris entre 3 et 4 heures. ( vrai ).
|
avancement (mol)
|
aA
|
+ bB |
initial
|
0
|
c0(A)(V1+V2)=c0V1 |
c0(B)(V1+V2)=4c0V1 |
final
|
x
|
c0V1 -ax
|
4c0V1 -bx |
A la fin : c(A) /c0(A)
= (c0V1 -ax) /((V1+V2)c0(A)) =(c0V1 -ax) /((5V1c0(A))
=(c0V1 -ax) /(c0V1)=1-ax /(c0V1) .
c(B) /c0(B) = (4c0V1 -bx) /((V1+V2)c0(B)) =(4c0V1 -bx) /((5V1c0(B))
=(4c0V1 -bx) /(4c0V1) = 1-bx /(4c0V1).
Hypothèse : la courbe 2 correspond à A : 1-ax /(c0V1) = 0,2 ; 1-bx /(4c0V1) = 0,6.
ax /(c0V1) = 0,8 ; bx /(4c0V1) = 0,4 ; ax /(c0V1) = 2 bx /(4c0V1) soit b = 2a.
Hypothèse : la courbe 2
correspond à B : 1-ax /(c0V1) = 0,6 ; 1-bx /(4c0V1) = 0,2.
ax /(c0V1) = 0,4 ; bx /(4c0V1) = 0,8 ; 2ax /(c0V1) = bx /(4c0V1) soit b = 8a ; imposible a et b
sont inférieurs à 5.
x = 0,8 c0V1/ a ; à t½ l'avancement vaut xt½=0,4 c0V1/
a.
A t½ : c0V1 -a xt½ = 0,6c0V1 ; c(A) /c0(A) = 0,6c0V1 /((V1+V2)c0(A)) = 0,6 ( courbe 2 ) ; l'abscisse
correspondante donne t½ compris entre 3 et4 heures.
B.
Le temps de demi-réaction est proche de 5 heures. ( faux ).
A
temps de demi-réaction ,l'avancement est égal à la moitié de
l'avancement final. Or la réaction est limitée, l'avancement final
n'est pas égal à 1.
C- Au temps t = 25
heures, il reste 60 % de l'un des réactifs et 20 % de l'autre. ( vrai ).
A la fin : c(A) /c0(A)
= 0,2 et c(B) /c0(B) = 0,6 ;
D- Les nombres
stoechiométrique a et b sont égaux. ( faux).
E- Les 4
affirmations précédentes sont fausses. ( faux ).
A-
La courbe 1 correspond au réactif
A. ( faux ).
B. Le réactif B est en excès. ( vrai ).
C- Si a = 1 alors b = 2. ( vrai ).
D-
Si on dilue le mélange réactionnel, les asymptotes horizontales aux
courbes 1 et 2 sont plus élevées sur le graphe. ( faux).
Les
rapports des concentrations ne dépendent pas de la dilution.
E- Les 4
affirmations précédentes sont fausses. ( faux ).
|
|
|