Séparer
les énantiomères de l'ibuprofène. Bac S Nlle Calédonie 2015
En poursuivant votre navigation sur ce site, vous acceptez l’utilisation de Cookies vous proposant des publicités adaptées à vos centres d’intérêts.
|
|
|
|
|
|
|
|
L'ibuprofène
est un anti-inflammatoire non stéroïdien. Il possède des propriétés
antalgiques,
antipyrétiques, anti-inflammatoires. On vend sous l'appellation
ibuprofène un produit de synthèse, correspondant au mélange équimolaire
de(S)-ibuprofène et de (R)-ibuprofène, ces deux molécules étant
énantiomères; ce mélange est donc qualifié de racémique. Or seul le
(S)-ibuprofène est responsable de l'effet clinique (160 fois plus
efficace que le (R)- ibuprofène in vitro). De plus, pris seul, le
(S)-ibuprofène agit plus rapidement et diminue les effets secondaires
par rapport à la prise du mélange racémique. Vendre dorénavant des
médicaments énantiomériquement purs, plutôt que des mélanges
racémiques, est une tendance forte de l'industrie pharmaceutique.
Le but de cet exercice est d'analyser une méthode permettant de
réaliser la séparation du (S)-ibuprofène du (R)-ibuprofène. La
qualité de cette séparation est évaluée à l'aide d'une grandeur appelée
excès énantiomérique .
L'excès
énantiomérique.
Soit un mélange contenant 2 énantiomères notés R et S. L'excès
énantiomérique du mélange, noté ee et exprimé en %, est donné par la
relation:
ee= |nR -ns| /(nR+nS)x100
où nR et ns sont
respectivement les quantités de matière des énantiomères R et S.
Mélange
racémique présent dans l'ibuprofène.
1.1. Justifier que
les molécules (S)-ibuprofène et (R)-ibuprofène sont des énantiomères.
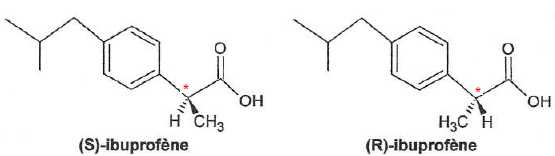
Les deux molécules sont énantiomères
: elles ne se différencient que par la disposition spatiale des groupes
fixés sur le carbone asymétrique. Elles sont image l'une de l'autre
dans un miroir plan.
1.2.
Indiquer la valeur de l'excès énantiomérique ee de l'ibuprofène.
Pour un mélange racémique, nR=ns et ee = 0.
1.3. Quelle
devrait être la valeur de l'excès énantiomérique ee pour un médicament énantiomériquement pur ?
ns=1 ; nR =0 ; ee = 100.
1.4. Citer
deux techniques de séparation classiques en chimie. Indiquer pour
quelles raisons ces techniques ne
permettent pas de séparer le (S)-ibuprofène du (R)-ibuprofène d'un
mélange.
Deux
énantiomères possèdent les mêmes propriétés chimique et physique (
excepté l'action sur la lumière polarisée ). Les techniques classiques
( Chromatographie, distillation, filtration. ), ne sont pas utilisables.
Étude d'une stratégie de séparation du (S)-ibuprofène et du (R)-ibuprofène.Réaction d'estérification de l'ibuprofène.Les deux énantiomères de l'ibuprofène peuvent réagir avec un alcool R-OH pour donner un ester et de l'eau. Cette réaction chimique, appelée réaction d'estérification, est extrêmement lente et limitée à température ambiante.
La
présence dans le mélange réactionnel d'une enzyme, la Candida Rugosa
Lipase, notée CRL7, permet de diminuer la durée de la réaction
d'estérification du (S)-ibuprofène seulement. l'équation de la réaction
d'estérification est la suivante :
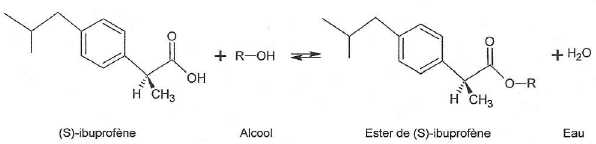
L'estérification
du (R)-ibuprofène reste très lente, au point que l'on peut considérer
qu'il ne se forme pas d'ester du (R)-ibuprofène, même au bout de 12 h.
|
| .
. |
|
|
Pour séparer les deux énantiomères, on met en oeuvre le protocole décrit ci-après:
Protocole de séparation des énantiomères de l'ibuprofène.
Étape 1 : on laisse réagir pendant 12 h et sous agitation un mélange réactionnel contenant:
5,0 ml de solvant ; 0,100 mmol d'ibuprofène ; 1,00 mmol d'alcool ;
0,1 g de CRl7 introduit à l'instant t = 0.
Étape 2 :
au bout de 12 h, on réalise une analyse du mélange réactionnel par une
technique adaptée afin dedéterminer la quantité de matière de
(R)-ibuprofène et celle de (S)-ibuprofène restantes dans le mélange
réactionnel.
Étape 3 : la quantité d'ester de (S)-ibuprofène produite après 12 h de réaction est extraite du mélange réactionnel par distillation.
Étape 4
: l'ester de (S)-ibuprofène récupéré est transformé intégralement en
(S)-ibuprofène par hydrolyse, réaction inverse de l'estérification.
2.1.
Recopier la formule du (S)-ibuprofène, entourer le(s) groupe(s)
caractéristique(s) présent(s) et nommer la(es) famille(s) chimique(s)
correspondante(s).
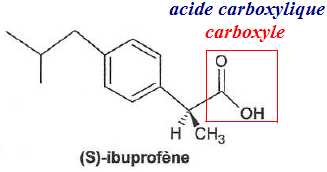
2.2. Y a-t-il lors de la réaction d'estérification précédente, modification de chaîne ou de groupe
caractéristique? Justifier.
La chaîne carbonée de l'ibuprofène n'est pas modifiée. Le groupe caractéristique est modifié ( on obtient le groupe ester.
2.3. Pourquoi l'enzyme CRL7 n'apparaît-elle pas dans l'équation de la réaction d'estérification ?
L'enzyme CRL7 joue le rôle de catalyseur stéréosélectif.
Le
protocole de séparation est réalisé à une température e = 50°C, en
utilisant pour alcool le méthanol et pour solvant l'isooctane.
L'analyse réalisée lors de "étape 2 indique qu'au bout de 12 h, le
mélange réactionnel contient le (R)-ibuprofène et 0,012 mmol de
(S)-ibuprofène.
2.4. Dans ces conditions, calculer la valeur de l'excès énantiomérique ee du mélange réactionnel à l'instant t=12h.
Initialement il y avait 0,050 mmol de chaque énantiomère.
A l'instant t = 12 h, nR = 0,050 mmol ; ns = 0,012 ;
ee = (0,050-0,012) *100 / (0,050+0,012) = 61.
2.5.
Déterminer la quantité de matière de (S)-ibuprofène qu'on peut
récupérer par hydrolyse de l'ester de (S)-ibuprofène extrait à l'étape
3 ?
Il s'est formé 0,050-0,012 = 0,038 mmol d'ester ; après hydrolyse, on peut récupérer au mieux 0,038 mmol de (S)-ibuprofène.
2.6. Quelle serait la valeur de l'excès énantiomérique ee du mélange réactionnel si la réaction
d'estérification était totale ?
A l'instant t = 12 h, nR = 0,050 mmol ; ns = 0,0 ; ee = 100.
|
|
|
|
Optimisation des conditions expérimentales de séparation des énantiomères de l'ibuprofène.
Afin
d'améliorer la séparation des énantiomères de l'ibuprofène, une équipe
de chercheurs a étudié l'influence de différents paramètres sur la
réaction d'estérification de l'ibuprofène du protocole de séparation.
3.1. Donner la formule topologique de l'isooctane et le nom de l'isoamylol en nomenclature officielle.
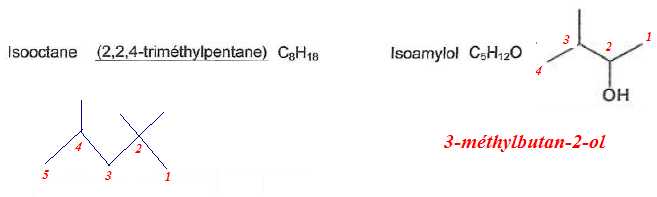
3.2. Pour chaque série de mesures, formuler une hypothèse que la série permet de tester.
Série 1 : le solvant organique a -t-il une influence ?.
Série 2 : l'alcool R-OH a -t-il une influence ?
Série 3 : la quantité initiale de matière d'alcool ( excès d'alcool ) a-t-elle une influence ?
Série 4 : quel est le rôle de la température ?
3.3.
Quelle classe d'alcool semble être à exclure pour réaliser la
séparation des énantiomères de l'ibuprofène ? Comment pourrait-on
conforter ce résultat ?
Un alcool tertiaire est à exclure. Dans ce cas ee = 0.
On admettra que l'ester de (S)-ibuprofène peut toujours être séparé du mélange réactionnel.
3.4.
À partir des résultats de l'équipe de chercheurs, préciser quelles
pourraient être les conditions expérimentales les plus favorables pour
séparer les énantiomères de l'ibuprofène selon le protocole de
séparation.
Solvant organique : isooctane.
Alcool ROH : isooctanol.
Ratio molaire 10.
Température 50°C.
3.5.
Quel volume de l'alcool choisi à la question 3.4. faut-il prélever pour
réaliser la séparation des énantiomères de l'ibuprofène dans les
conditions du protocole qui a été précisé ?
n = 1,00 mmol d'isooctanol. C8H18O ( M =8*12+18+16=130 g/mol ; 0,832 g / mL)
m = nM = 1,00 *0,130 =0,130 g ;
V = 0,130 / 0,832 =0,156 mL.
|
|
|
|