Dosage des
nitrites dans l'eau, gamme d'étalonnage. Olympiades chimie
En poursuivant votre navigation sur ce site, vous acceptez l’utilisation de Cookies vous proposant des publicités adaptées à vos centres d’intérêts.
|
|
|
|
|
|
|
Dosage en
réalisant une gamme d'étalonnage.
À partir d'une solution mère (S) à la concentration C = 10,0 mg/L en
ions nitrite, préparer par dilution 100 mL de solution étalon (Se)
à Ce=1,00 mg/L.
Quel
matériel faut-il utiliser ? Comment procéder
?
Facteur de dilution : F = C/Ce = 10. Fiole jaugée de 100,0
mL ; pipette jaugée de 10,0 mL+ dispositif d'aspiration ; de l'eau
distilée.
Rincer la pipette à l'eau distillée puis avec la solution mère ; rincer
la fiole jaugée avec de l'eau distillée.
Prélever 10,0 mL de solution mère à l'aide de la pipette jaugée et
placer le prélevementdans la fiole jaugée.
Complèter jusqu'au trait de jauge avec de l'eau distillée ; boucher et
rendre homogène.
Numéroter 7 tubes à essais de 0 à 6.
Introduire dans les 6 premiers tubes à essais 0, 2, 4, 6, 8, 10 mL de
solution étalon.
Compléter chaque tubes à 10 mL avec de l'eau distillée.
Dans le tube n°6, introduire 10 mL d'eau à doser
Ajouter dans chaque tubes 0,2 mL de réactif de diazotation, boucher et
homogénéiser.
Laisser la coloration se développer pendant environ 30 minutes.
Compléter
le tableau ci-dessous.
Tubes
|
0
( témoins )
|
1
|
2
|
3
|
4
|
5
|
Volume
solution Se (mL)
|
0
|
2
|
4
|
6
|
8
|
10
|
Volume
eau distillée ( mL)
|
10
|
8
|
6
|
4
|
2
|
0
|
Réactif
( mL)
|
0,2
|
Concentration
en ion nitrite ( mg/L)
|
0,000
|
2*1,00
/ 10,2
=0,196
|
4*1,00
/10,2
=0,392
|
0,588
|
0,784
|
0,980
|
On
donne le spectre d'une des solutions obtenues.
À quelle longueur
d'onde doit-on mesurer l'absorbance des solutions ?
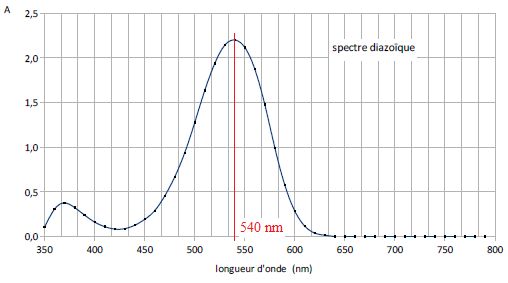
Pour une meilleure précision, on travaille au maximum d'absorption.
À
quoi sert la solution préparée dans le tube n°0 ?
Ce tube ne contient pas d'ion nitrite ; il sert à "faire le blanc".
Pourquoi
la solution est-elle rose ?
Le maximum d'absorption se situe vers 540 nm ( vert ). La solution
possède la couleur complémentaire du vert, c'est à dire le pourpre.
|
| .
. |
|
|
Au bout
de 30 minutes de repos, on prépare 7 cuves spectrophotométriques avec
un peu de chacune des solutions
contenues dans les tubes 0 à 6.
On mesurer les absorbances à l'aide du spectrophotomètre réglé à la «
bonne » longueur d'onde.
Tubes
|
0
|
1
|
2
|
3
|
4
|
5
|
6
|
Concentration
nitrite ( mg/L)
|
0,00
|
0,196
|
0,392
|
0,588
|
0,784
|
0,980
|
??
|
Absorbance
A
|
0,00
|
0,071
|
0,169
|
0,270
|
0,371
|
0,469
|
0,227
|
Tracer
la graphe de l'absorbance en fonction de la concentration en ions
nitrite.
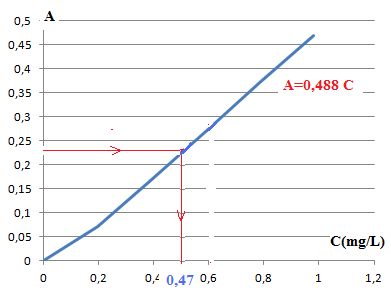
Que peut-on dire des
points expérimentaux ? À quelle loi cela correspond-il ?
Les points expérimentaux sont alignés. L'absorbance et la concentration
sont proportionnes. La loi de Beer-Lambert est vérifiée.
Déterminer
la concentration en ions nitrites dans l'eau et conclure.
Graphiquement on trouve c = 0,47 mg/L.
Par le calcul : c = 0,227 / 0,448 = 0,465 mg/L.
Cette valeur est supérieure à la norme ( 0,1 mg nitrite /L) :
l'eau n'est pas potable.
|
.
|
|
Dosage par la
méthode des ajouts dosés.
On ajoute de l'eau que l'on cherche à doser dans les tubes à essais.
On utilisera la solution étalon (Se) à 1,00 mg/L et le tube
témoins (tube n°0).
Préparer les tubes, de la même manière que pour la partie A, mais selon
les indications données dans le tableau ci-dessous.
Compléter la dernière ligne du tableau.
Tubes
|
1
|
2
|
3
|
4
|
5
|
Volume
solution Se (mL)
|
0
|
2
|
3
|
4
|
5
|
Volume
d'eau à doser (mL)
|
5
|
Volume
eau distillée ( mL)
|
5
|
3
|
2
|
1
|
0
|
Réactif
de diazotation( mL)
|
0,2
|
Caj
: concentration en ion nitrite ( mg/L)
provenant de (Se)
|
0,000
|
2*1,00
/ 10,2
=0,196
|
3*1,00
/10,2
=0,294
|
0,392
|
0,490
|
Laisser
la coloration se développer pendant environ 30 minutes.
Au bout de 30 minutes de repos, on
prépare 5 cuves spectrophotométriques avec un peu de chacune des
solutions
contenues dans les tubes 1 à 5.
On mesurer les absorbances à l'aide du spectrophotomètre réglé à la «
bonne » longueur d'onde.
Tubes
|
1
|
2
|
3
|
4
|
5
|
Caj (
mg/L)
|
0,00
|
0,196
|
0,294
|
0,392
|
0,490
|
Absorbance
A
|
0,111
|
0,206
|
0,251
|
0,296
|
0,343
|
Tracer
la graphe de l'absorbance en fonction de la concentration en ions
nitrite.
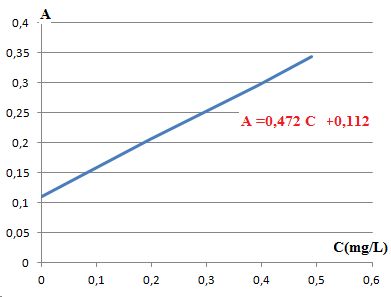
Donner
la relation liant l'absorbance A d'une des solutions préparée dans
cette partie et les concentrations Caj et Ci
(concentration en ions nitrite provenant de l'eau à doser). On notera k
le coefficient de proportionnalité. Calculer Ci et en déduire la
concentration CN en ions nitrite
dans l'eau.
A = kCtotale + b =k(Caj + Ci) +b = kCaj
+ kCi.
On identifie kCi à 0,112 et k à 0,472 L mol-1.
Ci = 0,112 / 0,472 =0,237 mg/L.
CN = 10,2 Ci /5 =10,2 *0,237/5 =0,484 mg/L.
Calculer
l'écart relatif entre les résultats trouvés par les deux méthodes.
(0,484-0,465) / 0,484 = 0,039 ( ~ 4 %).
L'erreur vient principalement de dilutions imprécises.
|
|
|