De
la composition d'un soda à sa consommation.
Bac S Métropole, Réunion 2015
En poursuivant votre navigation sur ce site, vous acceptez l’utilisation de Cookies vous proposant des publicités adaptées à vos centres d’intérêts.
|
|
|
|
|
|
|
Au XIXème
siècle, une boisson à base de feuilles de coca et de noix de cola était
préconisée par son
inventeur comme remède contre les problèmes gastriques. Cette boisson
est actuellement vendue comme soda. Sur l’étiquette de cette
boisson, on peut lire la liste d’ingrédients suivante : eau gazéifiée
au dioxyde de carbone ; sucre ; colorant (caramel) ; conservateur
(acide benzoïque) ; acidifiant (acide phosphorique) ; extraits végétaux
; arômes naturels (extraits végétaux dont caféine).
Dans cet exercice on s’intéresse à différentes espèces chimiques
présentes dans la composition de cette boisson.
Données
: pH de la boisson étudiée : 2,5 ; masse molaire de la caféine : M =
194,0 g.mol-1.
La Dose Journalière Admissible (DJA) est la dose maximale d’une
substance (exprimée en
mg par kg de masse corporelle et par jour) à laquelle on peut être
exposé de façon répétée sans
risque pour la santé :
|
Acide
phosphorique |
Acide
benzoïque |
Ion
benzoate |
Caféïne |
DJA
adulte
mg kg-1 jour-1 |
70 |
5 |
|
5 |
Solubilité
dans l'eau
g / L |
|
à
0°C |
à
25°C |
à
25°C |
|
|
1,7 |
3,4 |
650 |
|
Pour un enfant
de 30 kg, l’apport quotidien de caféine ne doit pas dépasser 75 mg, ce
qui
correspond environ à deux canettes de soda de 33 cL.
La caféine
La formule topologique de la molécule de
caféine est représentée. Recopier et compléter la formule
topologique de la molécule de caféine en faisant figurer les doublets
non liants.
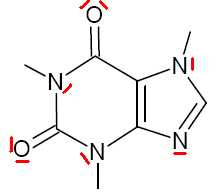
Déterminer la formule brute de la caféine. C8 H10O2N4.
Evaluer la concentration molaire approximative de la caféine dans le
soda.
75 mg dans
660mL soit 75 / M(caféïne) =75 / 194 =0,3866 mmol.
Concentration
en caféîne : 0,3866 / 660 = 5,86 10-4 ~5,9 10-4 mol / L.
L’acide
benzoïque.
L’acide benzoïque est un conservateur alimentaire souvent présent dans
les sodas. Une méthode de
synthèse de l’acide benzoïque peut s’effectuer en deux étapes au
laboratoire.
Étape (a) : obtention de l’ion benzoate à partir du benzonitrile
C7H5N(l) +H2O
+HO-aq ---> C7H5O2-aq
+ NH3aq.
Étape (b) : obtention de l’acide benzoïque par réaction de l’ion
benzoate avec l’ion oxonium
C7H5O2-aq
+H3O+aq --->C7H5O2H(s) + H2O.
Le but de cette
partie est d’analyser un protocole mis en oeuvre pour effectuer cette
synthèse au laboratoire ; la description des opérations
successives figure ci-dessous.
1. Dans un ballon de 100 mL, introduire un volume de 2,0 mL de
benzonitrile, un volume de 24 mL d’une solution aqueuse d’hydroxyde de
sodium à 100 g.L-1 et quelques grains de pierre
ponce.
2. Adapter un réfrigérant à eau, puis porter à ébullition pendant
plusieurs dizaines de minutes.
3. Une fois la réaction terminée, verser le contenu du ballon dans un
bécher, puis le refroidir à l’aide d’un bain de glace.
4. Ajouter de l’acide chlorhydrique froid en excès.
5. Filtrer sur Büchner (penser à laver les cristaux avec une solution
froide acidifiée).
6. Placer les cristaux à l’étuve (enceinte chauffante
thermostatée) pendant une heure.
7. Peser le produit obtenu.
|
| .
. |
|
|
Dans
l’opération 2 peut-on remplacer la solution aqueuse d’hydroxyde de
sodium par des pastilles
d’hydroxyde de sodium solide pour réaliser la synthèse ? Justifier.
L'eau figure
parmi les réactifs ( étape (a)). De plus la dissolution des pastilles
de soude est exothermique. Il vaut mieux ne pas les utiliser.
Quelles opérations correspondent à l’étape (a) de la synthèse de
l’acide benzoïque ?
Etape (a) :
opérations 1, 2 et 3. Etape
(b) :opération 4.
Donner deux raisons qui justifient l’utilisation du chauffage à reflux.
Le chauffage
à reflux permet d'accélérer la réaction ( la température est un facteur
cinétique ) tout en évitant les pertes de matière. Les vapeurs se
condensent dans le réfrigérant et retombent dans le milieu réactionnel.
Donner les rôles de chacune des opérations 4, 5 et 6 décrites
dans le protocole.
4 : étape b,
réaction acide base et obtention de l'acide benzoïque solide, celui-ci
étant quasiment insoluble
dans l'eau froide.
5 :
séparation du solide du liquide par filtration sous vide et lavage du
solide.
6 :
élimination des traces d'eau.
Quel critère doit on choisir pour régler une température de l’étuve
adaptée à l’opération . Justifier votre choix.
L'eau doit
s'évaporer ( T >100°C) et l'acide benzoïque doit rester solide (
T < 122 °C).
Citer deux méthodes permettant de vérifier la nature du produit obtenu.
Mesure du
point de fusion sur banc Kofler.
Chromatographie
sur couche mince.
Quelle masse maximale d’acide benzoïque peut être obtenue par la mise
en oeuvre de ce protocole ?
Quantité de matière initiale des réactifs :
n(benzonitrile)
= 2,0*1,01 / 103,04 = 1,96 10-2 mol ; n( soude) =
24*100/(1000*40)=0,060 mol..
L'hydroxyde
de sodium ( soude est en excès).
On peut
espérer obtenir au mieux 1,96 10-2 mol d'acide bezoïque soit
1,96 10-2 *122 ~2,4 g.
L'étiquette sur
la bouteille de soda indique la présence d’acide benzoïque comme
conservateur.
Est-ce bien sous cette forme que l'espèce prédomine dans cette boisson
? Justifier.
Le pH de la
boisson étant inférieur au pKa du couple acide benzoïque / ion
benzoate, l'acide benzoïque prédomine dans la boisson.
|
.
|
|
L’acide phosphorique.
Des études récentes laissent penser que l’acide phosphorique, H3PO4,
contenu dans certains sodas au cola est responsable d’un accroissement
des risques d’insuffisance rénale et d’ostéoporose s’il est consommé en
quantités trop importantes. Cette partie vise à évaluer la consommation
maximale de soda sans que l’acide phosphorique présente un
risque pour la santé.
Dosage de l’acide phosphorique dans le soda étudié.
Pour déterminer la concentration en acide phosphorique dans le soda, on
dégaze un volume V = 10,0 mL de soda afin d’éliminer le dioxyde de carbone dissous.
On réalise ensuite le titrage de la boisson dégazée par une solution
aqueuse d’hydroxyde de sodium Na+ (aq) ; HO-(aq) de concentration molaire C = 1,0×10-2 mol.L-1.
Le titrage est suivi par pH-métrie. On donne ci-dessous les mesures effectuées lors de ce titrage, V étant
le volume de solution d’hydroxyde de sodium versé.
| V(mL) | 0 | 1,0 | 2,0 | 3,0 | 4,0 | 5,0 | 6,0 | 7,0 | 8,0 | 9,0 | 10,0 | | pH | 2,9 | 3,1 | 3,2 | 3,3 | 3,6 | 4,5 | 5,6 | 6,2 | 6,3 | 6,4 | 6,4 |
Dans cette partie, on admet que seul le couple H3PO4 (aq)/H2PO4-
(aq intervient et que l’acide benzoïque étant en faible quantité,
sa présence influe très peu sur le dosage de l’acide phosphorique.
Combien de bouteilles de soda de 1,5 L une personne adulte peut-elle
consommer par jour, sans que l’acide phosphorique ne présente un risque
pour sa santé ?
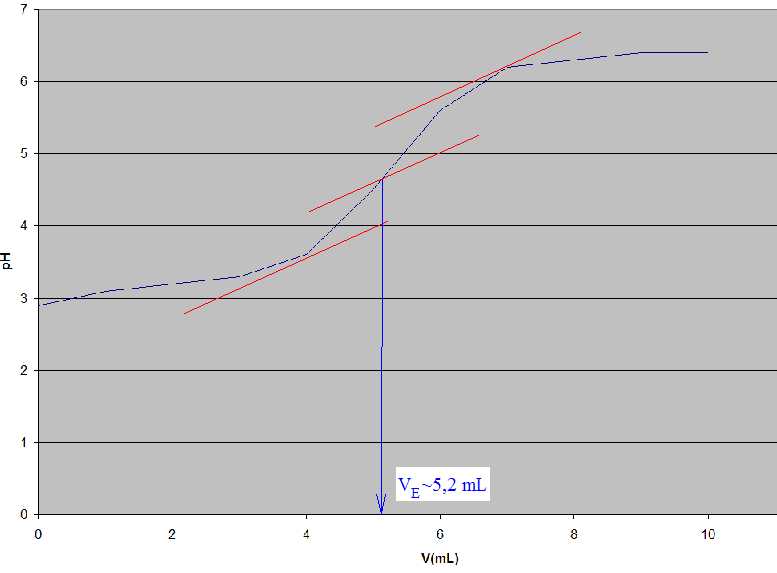
H3PO4 (aq) + HO-aq --> H2PO4- aq +H2O.
A l'équivalence : VE C = [H3PO4] V ; [H3PO4] = VE C / V = 5,2 *0,010 / 10 = 5,2 10-3 mol/L.
Soit 5,2 10-3 *98 ~0,51 g /L ~510 mg /L
soit 510*1,5 =765 mg par bouteille de 1,5 L de soda.
Pour un adulte de 75 kg, masse d'acide phosphorique absorbable par jour : 75 *70 = 5,3 103 mg.
Cet adulte peut donc boire 5,3 103 / 765 ~sept bouteilles de soda par jour.( cela n'est guère possible ).
|
|