Synthèse du
ß-bromostyrène, notions chimiques de base, concours inspecteur CCRF 2013
En poursuivant votre navigation sur ce site, vous acceptez l’utilisation de Cookies vous proposant des publicités adaptées à vos centres d’intérêts.
|
|
.
.
|
|
|
|
|
Le
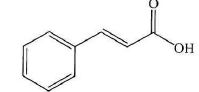
jasmin artificiel (ou β-bromostyrène), très odorant, peut être
synthétisé à partir de l'acide cinnamique ou acide
3-phénylprop-2-ènoïque (l'isomère E de ce composé a une odeur de
jasmin).
Sa
préparation se déroule alors en deux étapes :
1. Bromation de l’acide cinnamique (préparation de l'acide
2,3-dibromo-3-phénylpropanoïque).
2. Monodéshydrobromation du dérivé dibromé pour conduire au
β-bromostyrène
Quelle
est la configuration stéréochimique du composé représenté ?
Les deux groupes -COOH et C6H5- prioritaires sont
de part et d'autre de la double liaison C=C : donc composé trans ou (E).
On place 5,5 g de cet acide dans un ballon à fond rond de 100 mL,
additionnés de 50 mL d'éthoxyéthane. On ajoute avec précaution, et en
assurant une agitation, 10 mL d'une solution de dibrome dans l'éther, à
20% en volume (quantité de dibrome en excès par rapport à l'acide).
Quelle
verrerie va t-on utiliser pour prélever la solution de dibrome ?
Le volume V = 10 mL n'est pas très précis et le dibrome est en excès.
Ce volume peut être mesuré à l'aide d'une éprouvette gradué puis
introduit dans une ampoule de coulée fixée sur la ballon bicol.
L'acide se dissout dans la solution et on obtient une solution orange
foncé. On réalise ensuite un montage de distillation fractionnée à
l'aide d'une colonne de Vigreux comportant un réfrigérant à eau.
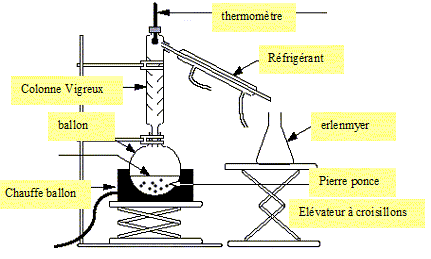
Faire
un schéma annoté de ce montage de distillation fractionnée, en
indiquant le nom des différents éléments du montage.
Quel est le rôle de
l'élévateur ? Expliquer.
L'élévateur permet de monter ou descendre le ballon afin de le
désolidariser du chauffe ballon et de laisser reforidir le ballon.
On utilise de la pierre-ponce. Quel est son rôle ?
Expliquer.
La pierre ponce poreuse régularise l'ébullition.
Après
refroidissement, on obtient dans le ballon un résidu solide. On ajoute
20 à 30 mL d'eau glacée
et on filtre sur Buchner en verre fritté, à l'aide d'une trompe à
eau.Les cristaux obtenus (blancs) sont lavés avec deux fois 10 mL d'eau
froide puis séchés à l'étuve à 100°C. Leur masse est de 10,3 g.
A
quoi sert le lavage à l'eau ?
Eliminer les impuretés solubles dans l'eau.
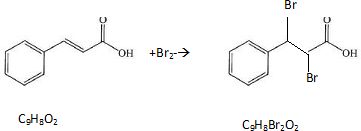
Donner
l'équation modélisant la réaction entre l'acide et le dibrome Br2. Indiquer dans
cette équation la formule brute des réactifs et du produit obtenu.
Calculer
le rendement r de la réaction.
Le rendement se calcule par rapport au réactif en défaut.
M(C9H8O2) = 9*12+8+2*16 =148 g/mol.
On peut espérer obtenir au mieux n = 5,5 / 148 =3,716 10-2
mol du produit.
M(C9H8Br2O2)
= 9*12+8+2*16 +2*80=308 g/mol.
Masse théorique du produit : 3,716
10-2 *308=11,45 g
Rendement : 10/11,45 =0,873 ou 87 %.
|
| .
. |
|
|
Le point de
fusion des cristaux obtenus est de 203°C. On obtient en réalité 50%
d'acide (2R,3S)- 2,3-dibromo-3-phénylpropanoïque (nommé S2)
et 50% d'acide (2S,3R)-2,3-dibromo-3- phénylpropanoïque (nommé S1).
Quelle
est l'orientation stéréochimique de l'addition de Br2 sur la
double liaison ?
L'addition du dibrome est trans du fait de la gène stérique autour de
la double liason C=C.
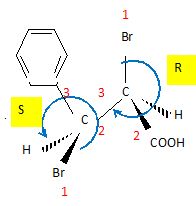
Représenter
l'acide (2R,3S)-2,3-dibromo-3-phénylpropanoïque (S2), en configuration
de Cram.
|
.
|
|
Mis
en présence de soude, ces cristaux (S1 et S2)
conduisent à l'anion de l'acide 2-bromocinnamique de configuration E
(composé B). La réaction se déroule en deux étapes :
1) la fonction acide carboxylique est déprotonée en présence des ions
hydroxydes
2) la réaction avec les ions HO- se fait ensuite selon
un mécanisme d'élimination de type E2.
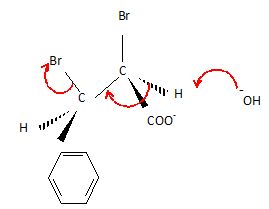
Représenter,
en configuration de Cram, le mécanisme de la réaction entre l'anion
carboxylate associé à S1 (ou à S2) et les ions HO-.
En
présence de carbonate de potassium dans l'acétone, S1 ou S2
éliminent une molécule de dioxyde de carbone et un ion bromure. La
transformation est stéréospécifique anti. Il se forme du β-
bromostyrène (composé C) de configuration Z (formule C6H5-CH=CHBr)
:
Donner
l'équation de la réaction modélisant cette transformation chimique en
indiquant les formules brutes des réactifs et des produits.
Réaction de type acide base : 2Ph-CHBr-CHBr-COOH
+ CO32- --> 2Ph-CHBr-CHBr-COO- +CO2
+ H2O.
Suivie de :
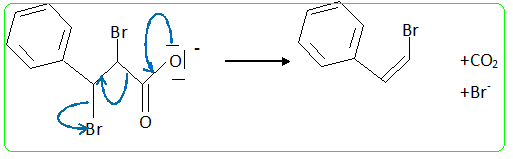
Enfin, les
cristaux S1 + S2 sont placés dans un erlenmeyer
de 250 mL. Dans un bêcher est introduit une quantité de matière en
excès de carbonate de potassium anhydre dissous dans 75 mL d'eau. On
introduit le contenu du bêcher dans l'erlenmeyer que l'on place sur une
plaque chauffante avec quelques grains de pierre ponce. Rapidement, le
solide disparaît et il se forme une huile de couleur jaune. On
refroidit le mélange dans un bain d'eau glacée et on extrait le composé
avec 2 fois 25 mL d'éther. Les extraits dans l'éther sont réunis dans
un erlenmeyer de 125 mL. On ajoute ensuite 2g de sulfate de magnésium
anhydre.
Quel
est le rôle du sulfate de magnésium anhydre ?
Le sulfate de magnésium anhydre est un déshydratant. Il élimine toute
trace d'eau.
La solution est ensuite filtrée et recueillie dans un ballon, puis
distillée au bain marie. On obtient 3,1g d'une huile à odeur de
jacinthe. (mélange de β-bromostyrène Z et E : composé (R1 +R2))
Calculer
le rendement de la formation de (R1 +R2) à partir de (S1 +S2).
M(C8H7Br) =12*8+7+80=183 g/mol.
Masse
théorique du produit : 3,716
10-2 *183=6,8 g
Rendement : 3,1 / 6,8 =0,456.
En
déduire le rendement de la formation de (R1 +R2) à partir de
l'acide 3-phényl-2- propénoïque.
0,873 *0,456 ~0,40.
|
Soit la molécule suivante : 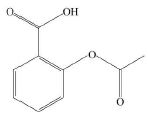
Nommer les deux fonctions chimiques présentes dans cette molécule.
Fonction acide carboxylique -COOH et fonction ester.
Que désigne un objet chiral? Citer un exemple d'objet chiral.
Un objet chiral n'est pas superposable à son image dans un miroir plan. Il ne présente aucune symétrie intrinsèque.
Une main droite, une chaussure.
Un objet possédant un plan ou un centre de symétrie est -il chiral ou achiral? Justifier.
Un objet possèdant une symétrie intrinsèque n'est pas chiral.
La molécule ci-dessus est -elle chirale? Justifier.
La molécule ci-dessus ne possède pas d'atome de carbone asymétrique, de
plus elle est quasiment plane. Cette molécule n'est pas chirale
La nomenclature chimique officielle de cette substance est l'acide O-acétylsalicylique.
Donner la formule brute et la formule développée de cette substance chimique.
C9H8O4.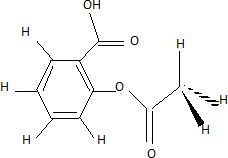
Quelle est le nom courant de cette substance et sa fonction ?
L'aspirine est un anti-inflammatoire.
Le numéro CAS de cette substance est le : 50-78-2
Que signifie le numéro CAS d'une substance chimique ?
Le numéro CAS permet d'identifier les espèces chimiques sans aucune
ambiguité.
Calculer la masse molaire de l'acide O-acétylsalicylique.
M =9*12+8+4*16=180 g/mol.
Quelle quantité de matière est contenue dans 0,5 g de ce composé ?
0,5 / 180 =2,778 10-3~2,8 10-3 mol. |
|
|