Spectroscopie : concentration d'une solution de permanganate : bts
Biotechnologie 2013.
En poursuivant votre navigation sur ce site, vous acceptez l’utilisation de Cookies vous proposant des publicités adaptées à vos centres d’intérêts.
|
|
.
|
|
|
|
|
On veut déterminer par spectroscopie UV-visible la concentration d'une solution aqueuse de permanganate de potassium..
Donner les quatre éléments principaux d'un spectrophotomètre.
Un spectrophotomètre est constitué d'une partie optique ( source, monochromateur à réseau,
cuve à échantillon) et d'une partie électronique ( photodiode, chaîne de
traitement du signal et affichage de l'absorbance). La formule fondamentale des réseaux plans est : sin q = sin i + k l/a.
Donner la signification des différents termes figurant dans cette formule et préciser les unités.
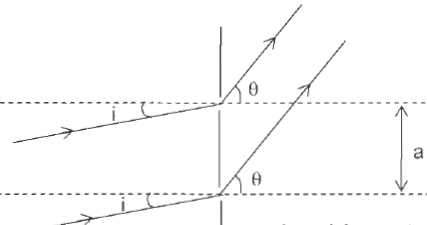
i : angle d'incidence ( degré) ; q : angle d'émergence ( degré) ;
l : (mètre) longueur d'onde de la lumière monochromatique éclairant le réseau ;
k : ordre de difraction ; k est un entier, positif, négatif ou nul.
a = 1/ n, pas du réseau (m) ; n : nombre de traits par unité de longueur.
Un
laboratoire possède un spectrophotomètre de haute qualité, dont le
monochromateur peut être utilisé dans l'ultraviolet, le visible et
l'infrarouge. Il comprend un jeu de plusieurs réseaux en fonction
de la longueur d'onde de travail. Pour ce dosage, on choisit un réseau
gravé ayant n = 500 traits par mm.
Le réseau est éclairé sous incidence normale par des radiations de longueur d'onde comprises entre l1 = 400 nm et l2 = 800 nm.
Définir et calculer le pas du réseau.
a = 1/n avec n = 500 *1000 = 5,0 105 traits par mètre.
a = 1/(5 105) =2,0 10-6 m.
|
| .
. |
|
|
Calculer dans le spectre d'ordre 1, les angles q1 et q2 pour les radiations de longueurs d'onde l1 et l2.
Le réseau est éclairé sous incidence normale ( sin i = sin 0 = 0).
A l'ordre 1, k = 1.
sin q1 = l1/a = 400 10-9 /(2 10-6) =0,20 ; q1 = 11,5°.
sin q2 = l2/a = 800 10-9 /(2 10-6) =0,40 ; q2 = 23,6°.
En déduire l'écart angulaire entre les deux radiations.
q2 - q1 =23,6-11,5 =12,1 °.
|
.
|
|
On donne le spectre d'absorption d'une solution aqueuse de permanganate de potassium. Cette solution est de couleur magenta.
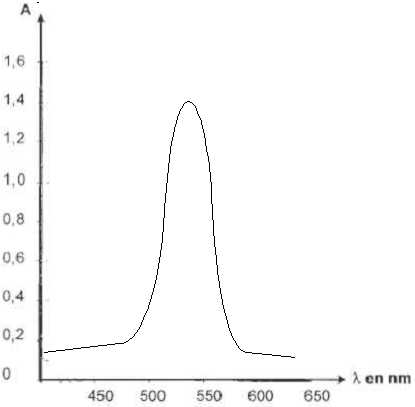
Justifier cette affirmation.
Une
solution contenant l'ion permanganate présente un maximum d'absorption
vers 540 nm ( vert). L'oeil perçoit la couleur complémentaire du vert,
c'est à dire le magenta.
A la longueur d'onde de travail ( lmax = 525 nm), le coefficient dextinction molaire vaut e = 2160 L mol-1 cm-1
et la longueur de la cuve est L = 1,00 cm. La solution aqueuse de
permanganate de potassium a une absorbance A =0,540. La realtion liant
l'absorbance et la transmittance T est A = -log T.
Calculer la transmittance de cette solution.
T = 10-A = 10-0,540 = 0,288.
Enoncer la loi de Beer-Lambert en défnissant les grandeurs introduites et en précisant leurs unité.
A=
elc
( A est
l'absorbance
ou densité
optique).
où e
est un coefficient caractéristique de la
substance appelé coefficient d'absorbance
(L mol-1
cm-1),
l est
l'épaisseur de la cuve
(cm) et
c la concentration de la solution
(mol/L).
Calculer la concentration molaire de cette solution.
c = A / (e L) =0,540 / (2160*1,00) =2,50 10-4 mol/L.
|
|