Eau potable ou non
? Bac S Pondichéry 2014
En poursuivant votre navigation sur ce site, vous acceptez l’utilisation de Cookies vous proposant des publicités adaptées à vos centres d’intérêts.
|
|
|
|
|
|
|
Le
paranitrophénol (PNP) est un polluant organique qui se forme lors de la
biodégradation de certains pesticides. Une exposition excessive à ce composé peut
provoquer une méthémoglobinémie : c’est-à-dire une diminution de la capacité du sang
à transporter le dioxygène dans les cellules. C’est la raison pour laquelle il faut
surveiller sa présence dans les eaux de boisson.
La valeur maximale de la concentration en PNP d’une eau potable
autorisée par la commission européenne est 0,1 μg.L-1. En revanche, le seuil fixé par
l’agence américaine de protection environnemental EPA (United States Environmental Protection
Agency) est 60 μg.L-1, tandis que la valeur tolérée par le conseil environnemental
brésilien est 100 μg.L-1.
A l’occasion d’un stage dans un laboratoire d’analyse chimique aux USA,
un groupe d’étudiants français met au point un protocole de dosage
spectrophotométrique du PNP et le met en oeuvre (document 1) pour étudier la potabilité d’une eau E
destinée à la consommation sur le continent américain.
Résolution de problème.
L’objectif de cet exercice est de répondre de manière argumentée à la
question que se posent les étudiants ingénieurs : l’eau analysée est-elle potable ?
Pour construire et développer votre argumentation, vous mobiliserez vos
connaissances et vous vous aiderez des deux documents fournis et des données, et vous
répondrez au préalable aux deux questions suivantes :
Dans les conditions expérimentales mises en oeuvre par les étudiants,
sous quelle forme se trouve le PNP dans les solutions ?
Le groupe hydroxyle –OH du paranitrophénol présente un caractère acide :
pKa(C6H5NO3 / C6H4NO3-) = 7,2.
A pH = 10,4, valeur supérieur au pKa, le PNP se trouve très majoritairement sous forme C6H4NO3-.
Pourquoi est-il justifié de choisir une radiation visible plutôt
qu’une radiation ultraviolette pour les mesures d’absorbance ?
Le spectre d'absorption du PNP en mileiu basique présente un
maximum d'absorption vers 400 nm. En se plaçant au maximum d'absorption
, on augmente la précision des mesures.
|
| .
. |
|
|
Document 1. Extrait du carnet de laboratoire rédigé par les étudiants.
On procède tout d’abord à une évaporation de l’eau E de manière à
accroître fortement la concentration en PNP. La solution S ainsi
obtenue est cent fois plus concentrée que la solution E.
À partir d'une solution aqueuse S0 de paranitrophénol de concentration C0 = 100 mg.L-1, on prépare cinq solutions filles Si de volume V = 100,0 mL en prélevant un volume Vi de solution S0 complété à 100,0 mL par une solution tampon de pH = 10,4.
On règle le spectrophotomètre sur la longueur d'onde l =
400 nm. On « effectue le blanc » de telle manière que l’absorbance soit
nulle avec la solution tampon de pH = 10,4. On mesure l'absorbance des
différentes solutions Si préparées. Les résultats des mesures sont regroupés dans le tableau suivant :
Solution
|
S1
|
S2
|
S3
|
S4
|
S5
|
Vi(mL)
|
1,0
|
2,0
|
3,0
|
5,0
|
7,5
|
A
|
0,128
|
0,255
|
0,386
|
0,637
|
0,955
|
On mélange 50,0 mL de la solution S avec 50,0 mL de solution tampon de
pH = 10,4 puis on mesure l'absorbance de la solution S' ainsi obtenue.
On obtient une absorbance A’ = 0,570 ± 0,010.
.
|
.
|
|
Document 2. Spectres d’absorption de solutions aqueuses de PNP en milieu acide et en milieu basique.
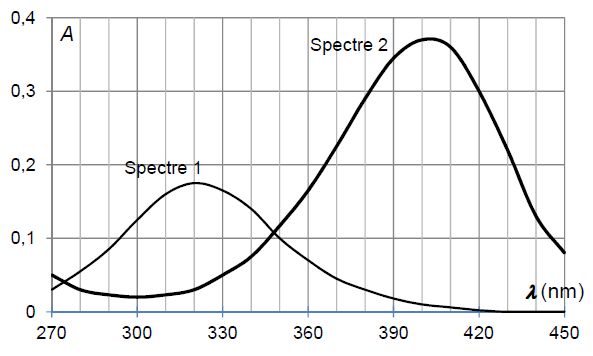
Spectre 1 : solution aqueuse de paranitrophénol de concentration molaire 2,0×10-5 mol.L-1 en milieu acide (pH = 5).
Spectre 2 : solution aqueuse de paranitrophénol de concentration molaire 2,0×10-5 mol.L-1 en milieu basique (pH = 10).
On réalise un dosage par étalonnage. Déterminons la concentration massique Ci (mgl/L) = C0Vi/V de chaque solution.
Solution
|
S1
|
S2
|
S3
|
S4
|
S5
|
Vi(mL)
|
1,0
|
2,0
|
3,0
|
5,0
|
7,5
|
| Ci (mgl/L) = C0Vi/V |
1,0
|
2,0
|
3,0
|
5,0
|
7,5
|
A
|
0,128
|
0,255
|
0,386
|
0,637
|
0,955
|
Tracer la courbe d'équation A = f(C).
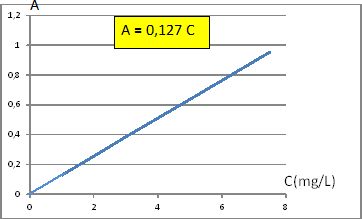
Concentration en PNP de la solution S' : C = A' / 0,127 =0,570 /0,127 =4,49 mg/L.
Concentration en PNP de la solution S : 4,49 * 2 = 8,98 mg/L
Concentration en PNP dans l'eau : 8,98 / 100 = 8,98 10-2 mg/L soit 89,8 µg/L.
Cette eau est déclarée non potable en Amérique du Nord.
|
|
|