Tensioactifs
; les carafes filtrantes : bac L - ES 2014
En poursuivant votre navigation sur ce site, vous acceptez l’utilisation de Cookies vous proposant des publicités adaptées ŕ vos centres d’intéręts.
|
|
|
|
|
Chocolat
Chantilly.
Il s'agit de réaliser une émulsion de type "matičre grasse dans l'eau".
Préciser
l'ingrédient qui joue le rôle de matičre grasse dans cette émulsion au
chocolat.
Le beurre de cacao joue le rôle de matičre grasse..
Justifier
la nécessité de chauffer le chocolat.
A température
ambiante le chocolat est un solide. Or une émulsion est un
mélange homogčne de deux substances liquides non
miscibles : suspension de gouttelettes de matičre grasse dans
l'eau,
stabilisées par des molécules tensioactives.
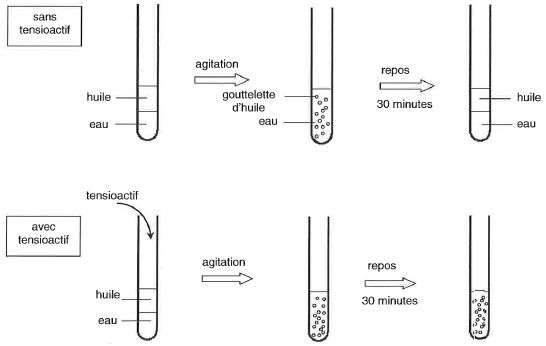
Décrire les
observations et en déduire la condition de stabilisation d'une émulsion.
Aprčs agitation les gouttelettes d'huile se dispersent dans l'eau.
Sans tensioactif, aprčs 30 minutes de repos, l'eau et l'huile se
séparent, ces deux liquides étant non miscibles ; l'huile, moins dense
que l'eau occupe la partie supérieure. Par contre en présence de
tensioactif, aprčs 30 minutes de repos, l'émulsion est stabilisée et
l'huile et l'eau ne se séparent pas.
Donner le
nom de la molécule qui, avant refroidissement, permettra de stabiliser
l'émulsion au chocolat.
La lécithine de soja ou du blanc d'oeuf est un tensioactif.
|
|
|
Interpréter
le rôle des molécules tensioactives dans la stabilisation de l'émulsion
de chocolat.
Les tensioactifs possčdent un
groupe caractéristique hydrophile et une
longue chaîne carbonée hydrophobe.
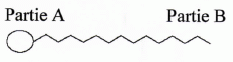
La partie A est hydrophile ; la
partie B est hydrophobe.
Lors de l'action d'un agent
tensio-actif il y a formation de micelles.
Le schéma
ci-dessous
représente une micelle de type " huile dans l'eau".
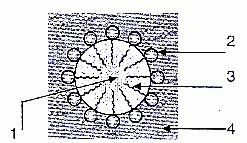
1 : huile
2 : partie hydrophile du tensioactif
3 : partie hydrophobe du tensio-actif
4 : eau.
Lors de la seconde étape " on pose la casserole contenant l'émulsion de
chocolat sur des glaçons et l'on fouette".
Justifier
la nécessité de fouetter le mélange et indiquer le rôle du
refroidissement.
Fouetter vigoureusement le mélange permet d'y incorporer des bulles
d'air, indispensables pour l'obtention d'une mousse. Sous la pression
atmosphérique ( 1 bar) le mélange chaud est ŕ l'état liquide. Lors du refroidissement la
matičre grasse cristallise ce qui stabilise les bulles d'air dans la
masse.
|
.
|
|
Les carafes
filtrantes.
Le filtre de la carafe permet de diminuer fortement la dureté de l'eau
en retenant certains ions.
Quels
sont les deux ions responsables de la dureté de l'eau ?
L'ion calcium Ca2+ et l'ion magnésium Mg2+ sont
responsables de la dureté de l'eau.
Un utilisateur de ce type carafe filtre son eau avant de la faire
bouillir.
Décrire
ce qu'il observera sur la résistance chauffante de la bouilloire si le
filtre n'est plus efficace.
En chauffant une eau dure, on observera un dépôt de calcaire, carbonate
de calcium sur la résistance de la bouilloire.
Dans la phase de traitement des eaux naturelles, on introduit du chlore.
Quel
est le rôle du chlore ?
Ce
traitement au chlore élimine toute forme de contamination par les
bactéries et les virus lors du transport de l'eau.
Le filtre de la carafe élimine le chlore( présent sous forme d'ion
hypochlorite et chlorure ).
Indiquer
la récaution ŕ prendre pour conserver pendant un ou deux jours une eau
filtrée.
Placer l'eau filtrée au réfrigérateur.
Changer réguličrement les cartouches filtrantes en les manipulant avec
des mains propres.
On veut tester la présence d'ion chlorure dans une eau préalablement
filtrée par la carafe.
Compléter
le schéma suivant.
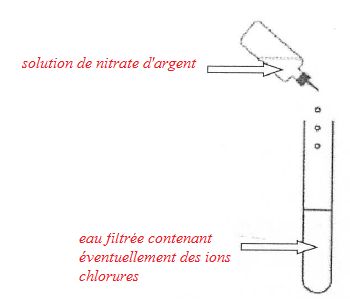
Lors de ce test, on a observé la formation d'un précipité blanc.
Evaluer
l'état de fonctionnement de la cartouche filtrante.
La présence d'un précipité blanc de chlorure d'argent indique la
présence d'ion chlorure dans l'eau filtrée. Le goűt de chlore
persiste dans l'eau filtrée, ce dernier n'étant pas totalement éliminé.
Expliquer
pourquoi ŕ l'heure actuelle l'achat d'une carafe filtrante n'est plus
utile pour se protéger des ions nitrate.
Les stations de traitement de l'eau se sont multipliées et les
captages d'eau potable pollués par les nitrates sont abandonnés.
|
|
|



