|
|
|
|
Question 8.
On rťalise une pile argent cuivre en associant :
- une demi-pile 1 constituťe d'une ťlectrode d'argent plongeant dans
une solution de nitrate d'argent.
- une demi-pile 2 constituťe d'une ťlectrode de cuivre plongeant dans
une solution de sulfate de cuivre (II).
On constate lors du fonctionnement de la pile que la solution dans
laquelle plonge l'ťlectrode de cuivre est de plus en plus foncťe. La
pile fonctionne durant 10 minutes et dťbite un courant d'intensitť I =
100 mA.
On prendra 1 F = NA e ~ 105 C mol-1.
M(Cu) = 63,5 g/mol ; M(Ag) = 108 g/mol.
A) La demi-pile 1 est le siŤge d'une rťduction. Vrai.
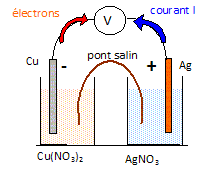
Oxydation du cuivre ŗ l'anode nťgative :
Cu(s) = Cu2+aq
+ 2e-.
Rťduction des ions argent
ŗ la cathode positive : 2Ag+aq
+ 2e- = 2Ag(s)
Bilan : Cu(s) +2Ag+aq=
Cu2+aq
+
2Ag(s).
B) La demi-pile 1 est le siŤge d'une oxydation. Faux.
C) L'ťlectrode d'argent constitue la cathode. Vrai.
D) Entre les deux demi-piles on utilise un fil
ťlectrique pour faire la jonction. Faux.
E)
Durant le temps de fonctionnement de cette pile la variation de masse
de l'ťlectrode de cuivre est Dm(Cu)
= 7,62 mg. Faux.
Quantitť d'ťlectricitť :
Q = I t = 0,100 *10*60 = 60 C.
Quantitť de matiŤre
d'ťlectrons : n(e-) = Q / F = 60 / 105
= 6 10-4 mol.
Quantitť de matiŤre de
cuivre : n(Cu) = Ĺn(e-) =3 10-4 mol.
La masse de cuivre diminue : Dm(Cu)
= -n(Cu) M(Cu) =
-3,10-4 *63,5 = -0,019 g ~ -19 mg.
F) Aucune proposition ne convient. Faux.
|
.
|
Question 9.
Le rouge de mťthyle est un indicateur colorť acido-basique. Son pKa est
ťgal ŗ 5,2. Sa teinte acide est rouge et sa teinte basique est jaune.
La formule topologique d'une des espŤces prťsente dans cet indicateur
est :
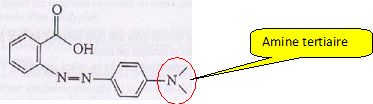
A) La molťcule reprťsentťe donne une teinte rouge ŗ la solution. Vrai.
On distingue le groupe
carboxyle -COOH prťsent en milieu acide, ŗ pH < pKa.
A pH > pKa,
l'ion carboxylate serait majotitaire et la solution serait jaune.
B) La molťcule prťsente une fonction amine secondaire. Faux.
C) La masse molaire de cette molťcule est M = 268 g/mol. Faux.
Un nombre impair d'atome
d'azote donne une masse molaire impaire.
M(C15H15O2N3)
=15*12 +15 +2*16 *3*14 =269 g/mol.
D) L'indicateur colorť teinte une solution aqueuse de chlorure de
sodium de concentration c = 0,010 mol/L en rouge. Faux.
Une solution aqueuse de
chlorure de sodium a un pH neutre ( pH = 7 ŗ 25 įC).
A pH supťrieur au pKa
de l'indicateur colorť la forme basique prťdomine et la solution est
teintťe en jaune.
E) Lorsque l'indicateur colorť est dans un milieu de pH = 7,2, la
proportion de l'espŤce acide est d'environ 1%. Vrai.
pH = pKa
+ log ( [A-] / [AH]) ; log ( [A-] / [AH]) = 7,2 -5,2 = 2 ; [A-] / [AH] = 100 ; [AH] = [A-]
/100.
F) Aucune affirmation correcte. Faux.
|
|
Question 10.
On considŤre une masse m d'ťthanol. On mťlange ce composť avec un excŤs
de dichromate de potassium acidifiť. On obtient alors un composť
organique unique notť A. La masse obtenue est mA = 30 g.
Dans un ballon on introduit 30 g de A et 74 g de butan-2-ol. On
maintient une ťbullition douce pendant une heure. On obtient alors un
composť B : l'ťthanoate de 1-mťthylpropyle. On suppose l'ťquilibre
atteint.
On prťlŤve alors le dixiŤme du milieu rťactionnel et on le dose par
titrage avec une solution de soude de concentration c = 0,50 mol/L.
L'indicateur colorť utilisť est le BBT.
Il faut verser un volume V = 20 mL de soude pour que le BBT change de
couleur.
A) A est un
aldehyde, l'ťthanal. Faux.
Un alcool primaire
conduit ŗ un acide carboxylique en prťsence d'un excŤs d'oxydant. A est
l'acide ťthanoÔque.
B) La masse moaire de A est ťgale ŗ 59 g/mol. Faux.
M(C2H4O2
) =2*12 +4+2*16 = 60 g/mol.
C) L'autre produit
obtenu lors de la rťaction entre A et le butan-2-ol est de l'eau. Vrai.
acide carboxylique + alcool = ester + eau.
D) A l'ťquilibre il
reste 0,10 mol de butan-2-ol. Faux.
n(A) i = 30 /
60 = 0,50 mol ; n(butan-2-ol) i = 74 / 74 = 1,0 mol.
L'alcool est en excŤs.
On dose l'acide
ťthanoÔque restant ŗ l'ťquilibre : n(A) restant = cV = 0,50
*0,020 =0,010 mol soit 0,10 mol de A dans tout le milieu rťactionnel.
0,40 mol de A a donc rťagi avec 0,4 mol de butan-2-ol : il reste donc
0,60 mol d'alcool ŗ l'ťquilibre.
E) Le rendement de
la rťaction est de 80 %. Vrai.
On calcule de rendement
par rapport au rťactif en dťfaut, ici "A".
A partir de 0,50 mol de A on peut espťrer obtenir au mieux 0,50 mol
d'ester ; or il ne s'en forme
que 0,40 mol.
F) Aucune proposition ne convient. Faux.
|
|

