|
|
|
|
Les acides organiques du vin tels que l'acide tartrique et l'acide malique peuvent Ítre dosťs par HPLC.
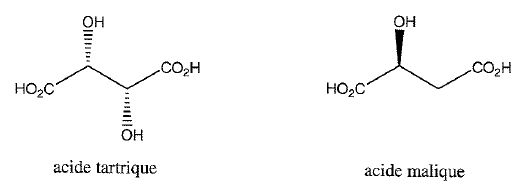
Donner leurs noms en nomenclature officielle ?
Acide 2, 3-dihydroxybutane-1,4-dioÔque ; acide 2-hydroxybutane-1,4-dioÔque
Ces
composťs possŤdent-ils des carbones asymťtriques ? Si oui, notez sur
les structures ci-dessous et prťciser leur(s) configuration(s).
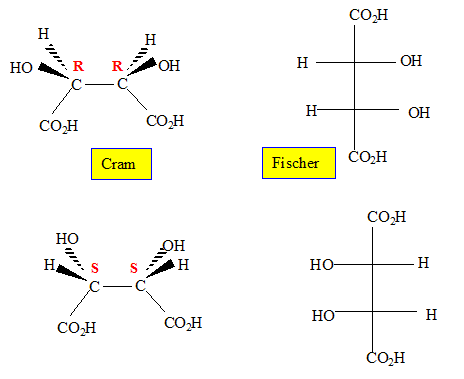
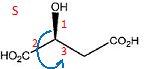
Ces composťs sont-ils optiquement actifs ?
Ces composťs ne possťdant aucun ťlťment de symťtrie sont optiquement actifs.
|
.
|
Ces composťs sont analysťs en HPLC dans les conditions suivantes : colonne C18, 5Ķm, 250 x 4, ťluant eau ŗ 0,2 % de H3PO4, dťbit 0,7 mL min-1, boucle d'injection 10 ĶL, dťtection UV 210 nm. On observe deux pics 1 et 2 de temps de rťtention t1 = 3,5 min et t2 = 4,2 min et de largeur de pic de base w1 = 0,15 min et w2 =0,16 min.
Que signifie le terme C18 ?
Les groupes alkyles greffťs sur la phase stationnaire comptent 18 atomes de
carbone.
S'agit-il d'une chromatographie d'adsorption ou de partage ? Justifier.
La chromatographie de partage :
Elle est basťe sur la
diffťrence de solubilitť du solutť dans la phase mobile et la phase
stationnaire
C'est une
chromatographie liquide-liquide. La phase stationnaire est un liquide fixť sur
un support inerte. Cette chromatographie est ainsi dťnommťe car elle est basťe
sur le partage du solutť dans les deux phases liquides .
Il s'agit d'une chromatographie d'adsorption
:
C'est une chromatographie liquide-solide. La phase stationnaire est un
adsorbant solide polaire.
- La chromatographie d'adsorption en phase inverse
:
C'est une chromatographie liquide-solide dans laquelle la phase
stationnaire est apolaire.
Pourquoi met-on de l'acide dans l'ťluant ?
En milieu basique,
l'acide carboxylique serait en partie sous forme d'ion carboxylate.Le milieu acide ťvite cette
rťaction.
Attribuer ŗ l'acide tartrique et ŗ l'acide malique leurs temps de rťtention. Justifier l'ordre d'ťlution.
La phase stationnaire est apolaire ; la phase mobile est polaire : les espŤces
les plus polaires migrent le plus vite.
Dans l'ordre, du plus rapide au
moins rapide : acide tartrique ( t1 = 3,5 min), acide malique ( t2 = 4,2 min).
A quoi est due l'absorbance ŗ 210 nm ?
Doublet ťlectronique libre de l'oxygŤne ; transition n - s*.
Afin de juger l'efficacitť de l'analyse, vous devez dťterminer le nombre de plateaux thťoriques N.
Quelle formule allez-vous utiliser ? Calculez N et H ( hauteur ťquivalente ŗ un plateau thťorique ) pour l'acide tartrique.
N = 5,54 (t /wĹ)2 = 16(t /w0)2 = avec t : temps de rťtention et wĹ : largeur du pic ŗ mi-hauteur ; largeur de la base du pic w0 = 1,7 wĹ si le pic est gaussien.
N = 16 (3,5 / 0,15)2 ~8,7 103.
H = L/N avec L longueur de la colonne. Pour une colonne de longueur 1 m, H = 1,1 10-4 m.
Afin de quantifier ces deux acides dans diffťrents ťchantillons, on se propose de rťaliser un ťtalonnage.
Quel type d'ťtalonnage prťconisez-vous ? Justifiez et dťcrivez la rťalťtalonnage.
L'aire d'un pic est proportionnelle ŗ la concentration ou ŗ la quantitť de produit analysť. Le volume injectť sera constant.
On compare la rťponse du ou des produits ŗ analyser ŗ celle d'un ťtalon interne.
Mťthode de l'ťtalon interne : une solution ťtalon est prťparťe avec le
ou les produits que l'on veut doser. Dans l'ťchantillon contenant les
masses m1, m2... de solutťs, on ajoute me de l'ťtalon.
|
Si
vous devez comparer deux conditions d'analyse diffťrentes, la plus
efficace est-elle celle qui donne le plus grand ou le plus petit nombre
de plateaux ?
Plus le pic est fin,plus le nombre de plateaux thťorique est grand et plus la chromatographie est efficace.
Comment dťterminer expťrimentalement le temps mort de cette analyse ?
Le temps mort tm
est le temps mis par un composť non retenu par la phase stationnaire
pour traverser la colonne (temps passť uniquement dans la phase mobile).
Injecter un produit non retenu par la colonne.
D'autres acides sont prťsents dans le vin. L'aciditť totale d'un vin
est la somme des acides titrables, quand on amŤne le vin ŗ pH =7 par
addition d'une solution de soude. L'acide carbonique n'est pas compris
dans l'aciditť totale. Comment ťliminer l'acide carbonique du vin ?
Porter le vin ŗ ťbulition pendant quelques minutes. Le dioxyde de carbone dissous se dťgage.
L'aciditť totale doit Ítre exprimťe en gramme d'acide tartrique par
litre de vin. Le dosage de 5 mL de vin par la soude NaOH ŗ 0,1 mol/L en
prťsence de BBT donne un volume de 9 mL.
Exprimer l'aciditť totale du vin en g/L d'acide tartrique.
n(soude) = 0,1 *9 = 0,9 mmol.
L'acide tartrique est un diacide : n( acide tartrique) = Ĺn(soude) = 0,45 mmol dans 5 mL de vin soit 0,45/5 =0,09 mol/L.
M( acide tartrique ) = 4*12+6+6*16 = 150 g/mol soit 0,09*150 =13,5 g/L.
Parmi les acides carboxyliques ci-dessous, quel composť prťsente l'aciditť la plus forte ? La moins forte ? Justifier en faisant appel aux effets ťlectroniques.
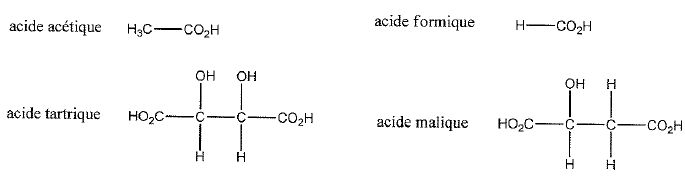
L'acide est d'autant plus fort que l'hydrogŤne du goupe OH est plus mobile, plus appauvri en ťlectrons.
OH est attracteur d'ťlectrons, CH3 est donneur d'ťlectrons, par suite l'acide tartrique est le pus fort, l'acide acťtique le plus faible.
Vous ne disposez pas d'une colonne C18, mais d'une colonne de silice pour effectuer cette analyse.
Proposez une modification chimique des acides malique et tartrique pour leur analyse sur colonne de silice.
La colonne de silice est polaire ; l'ťluant sera apolaire ; estťrifier
les fonctions acide carboxylique de l'acide tartrique et de
l'acide malique.
|
|



