|
|
|
|
La benzocaďne fait partie du groupe des allergčnes.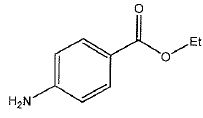
C'est un anesthésique local essentiellement utilisé pour une action en
surface sur la peau ou sur les muqueuses. Le produit de départ utilisé
pour cette synthčse est le paranitrotolučne A.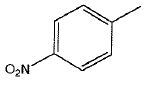
Combien ce composé possčde-t-il de carbone asymétrique ?
Auncun carbone tétragonal lié ŕ quatre atomes ou groupe d'atomes différents.
Comment obtenir le composé A ŕ partir du benzčne.
Réaction de Friedel et Craft pour obtenir le tolučne puis nitration du tolučne.
Pourquoi est-il interdit au laboratoir de synthétiser le para-nitrotolučne ŕ partir du benzčne ?
On peut former du trinitrotolučne explosif.
Le para-nitrotolučne est toxique et dangereux. C'est un composé volatil.
Quelles précautions appliqueriez-vous pour manipuler ce composé ?
Port de blouse, gants et lunette de sécurité ; travail sous hotte aspirante.
Le paranitrotolučne réagit avec KMnO4 :

KMnO4 est utilisé en large excčs pour obtenir une réaction totale.
Quel est le rôle de KMnO4 ? Dans quelle catégorie classeriez-vous cette réaction ?
KMnO4 est un oxydant, il s'agit d'une réaction d'oxydation de la chaine latérale.
Proposez une méthode de suivi de la réaction.
Le permanganate est la seule espčce fortement colorée en violet : suivi spectrophotométrique ŕ l = 550 nm, longueur d'onde oů KMnO4 présente un maximum d'absorption.
B est obtenu pur.
Quelles caractéristiques spectrales permettent d'affirmer sans ambiguité la formation de B ?
IR, vibration de valence de la liaison C=O du groupe carboxyle vers 1680 cm-1 ( bande forte ).
Vers 3000 - 3500 cm-1, vibration de valence du groupe OH ( bande large due ŕ l'existence de liaisons hydrogčne ).
Cette réaction fournit 12 g d'acide B avec un rendement de 85 % en produit pur.
Quelle quantité de para-tolučne A a-t-on utilisé ?
M(A) =7*12 +8+14+2*16=138 g/mol ; M(B) =7*12+6+14+4*16 =168 g/mol.
n(B) = n(A) = 12/168 =0,0714 mol.
m(A) = 0,0714*138 =9,86 g pour un rendement de 100 %.
Prendre en compte le rendement : 9,86 / 0,85 =11,6 g.
|
.
|
Proposer une méthode de purification de ce genre de composé.
Purification par recristallisation.
Le composé B réagit avec l'éthanol en milieu acide.
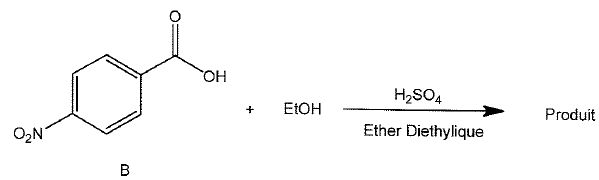
Dans un ballon de 250 mL contenant 100 mL d'éther, équipé d'un
réfrigérant ŕ reflux, d'une ampoule isobare et d'un systčme
d'agitation, on introduit 6,8 g de B et 60 mL d'alcool absolu. On
ajoute lentement, en agitant 8 mL d'acide sulfurique concentré et on
chauffe ŕ reflux pendant 45 minutes.
On refroidit ŕ température ambiante ; on verse le contenu du ballon sur
100 mL d'une solution de soude ŕ 10 % et 100 g de glace pillée, en
agitant vigoureusement.
On filtre sur büchner, puis on rince ŕ l'eau glacée.
Quel produit obtientdra-t-on ?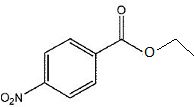
Le produit obtenu est-il la benzocaďne ? Si la réponse est non, quel type de réaction faut-il effectuer.
Non, pour cela il faut réduire le groupe nitro NO2 en amine NH2.
|
|




