|
|
|
|
Constitution de l'atome.
l'atome d'oxygŤne a pour symbole 168O. L'ion oxyde s'ťcrit O2-.
Indiquer le nombre de neutrons, de protons et d'ťlectrons de cet ion.
16-8 = 8 neutrons ; 8 protons et 8+2 = 10 ťlectrons.
Quel est le type de rťaction subie par l'ťlťment O pour former l'ion O2- ?
Latome gagne deux ťlectrons pour former l'ion oxyde ; un gain d'ťlectron correspond ŗ une rťduction.
Evaluer la masse d'une mole d'atome d'oxygŤne. Commenter le rťsultat.
mproton ~mneutron ~1,67 10-27 kg ; mťlectron = 9,1 10-31 kg ; NA = 6,02 1023 mol-1.
(16*1,67 10-27 +8*9,1 10-31 )*6,02 1023 =1,61 10-2 kg/mol =16,1 g/mol.
La masse d'un atome est infťrieure ŗ la masse de ces constituants isolťs et au repos.
Donner l'ťcriture symbolique de l'atome de cuivre sachant qu'il possŤde 34 neutrons et que son nombre de masse est 63.
Z = 63-34 = 29 ; A = 63 ; 6329Cu.
Dťfinir "isotopes".
Deux isotopes ne se diffťrencient que par leur nombre de neutrons. Ils possŤdent le mÍme numťro atomique Z.
Rťpondre par vrai ou faux aux propositions suivantes :
Le noyaux de l'atome contient des protons et des ťlectrons. ( faux) ... des protons et des neutrons.
Dans un atome le nombre de protons et toujours ťgal au nombre d'ťlectrons ( Vrai) ... l'atome est ťlectriquement neutre.
En gagant des ťlectrons un atome se transforme en cation. ( faux) ... en anion nťgatif.
Un ťlectron porte une charge positive. ( faux ).
L'ion Zn2+ provient d'une oxydation du zinc. ( vrai) ... une oxydation correspond ŗ une perte d'ťlectrons.
Un anion est un atome ayant gagnť un ou plusieurs ťlectrons. ( vrai).
Tous les isotopes sont radioactifs. ( faux ).
Donner le symbole chimique des ťlťments suivants.
Azote N ; mercure Hg ; potassium K ; magnťsium Mg.
Donner le nom associť aux symboles suivants.
Na sodium ; Mn manganŤse ; Sn ťtain ; Cd cadmium.
Donner le nom des corps dont les formules sont.
C6H6 benzŤne ; HNO3 acide nitrique ; D2O eau lourde ; CH4 mťthane.
Donner les formules chimiques des produits dont les noms sont :
Sulfate de cuivre CuSO4 ; acide nitreux HNO2 ; acide acťtique CH3-COOH ; potasse caustique KOH.
|
Rťactions chimiques.
Equilibrer les rťactions suivantes :
4CO + Fe3O4 --> 4CO2 + 3Fe.
Cu2S + 2Cu2O --> 6Cu + SO2.
2MnO4- + 5H2SO3 + 6H+ --> 2Mn2+ + 5H2SO4 + 3H2O.
C4H10 + 6,5O2 --> 4 CO2 + 5 H2O.
2S2O32- + I2 --> S4O62- + 2I-.
Le diode est rťduit I2 + 2e- = 2I-.
Ecrire l'ťquation de la rťaction acido-basique entre une solution aqueuse d'ammoniac et l'acide chlorhydrique.
NH3aq + H3O+aq + Cl-aq -->NH4+aq + Cl-aq + H2O(l).
|
Solutions, concentrations.
Le propane a pour formule C3H8. Calculer sa masse molaire.
M = 3*12+8 = 44 g/mol.
Une bouteille contient 13 kg de propane.
Calculer la quantitť de matiŤre correspondante.
n = m / M = 13 000 /44 =2,9545 102~3,0 102 mol.
On dissout 2 g de pastilles de soude dans 250 mL d'eau.
Calculer la concentration massique ( kg m-3) et molaire ( mol/L) de la solution de soude.
M(NaOH) = 23 +16+1 = 40 g/mol.
n = m / M = 2/40 = 0,05 mol dans 0,25 L ; C = 0,05 / 0,25 =0,2 mol/L.
0,2 *40 = 8 g /L ou 8 10-3 / (10-3) = 8 kg m-3.
Calculer le pH de la solution.
pH d'une base forte : 14 + log C = 14 + log 0,2 =13,3.
On veut prťparer un volume V2 = 2 L d'une solution d'ammoniac NH3 de concentration C2 = 0,10 mol/L. On dispose pour cela d'une solution commerciale de concentration C1 = 15,50 mol/L. Quel volume V1 de solution commerciale faut-il prťlever ?
Facteur de dilution F = 15,50 / 0,10 = 155.
V1 = V2 / 155 =12,9 ~13 mL.
Chimie organique.
On fait rťagir de l'acide heptanoÔque C7O2H14 sur de l'ťthanol. On obtient un arŰme artificiel qui a l'odeur de cognac.
Ecrire la formule semi-dťveloppťe de l'acide heptanoÔque.
CH3-CH2-CH2-CH2-CH2-CH2-COOH
Quel est le groupement fonctionnel caractťristique des acides carboxyliques ?
Groupe carboxyle -COOH.
Ecrire la formule semi-dťveloppťe de l'ťthanol.
CH3-CH2OH.
Ecrire l'ťquation de la rťaction entre l'acide heptanoÔque et l'ťthanol.
CH3-CH2-CH2-CH2-CH2-CH2-COOH + CH3-CH2OH = CH3-CH2-CH2-CH2-CH2-CH2-COO-CH2-CH3 + H2O.
Rťpondre par vrai ou faux.
La rťaction entre l'acide heptanoÔque et l'ťthanol s'appelle une estťrification. Vrai.
La rťaction entre l'acide heptanoÔque et l'ťthanol s'appelle une saponification. Faux.
La rťaction inverse d'une estťrification est une saponification. Faux. ... une hydrolyse de l'ester.
La rťaction inverse d'une estťrification est une rťacvtion d'hydrolyse. Vrai.
|
Connaissance du matťriel.
Nommer le matťriel ci-dessous et indiquer succinctement son usage.
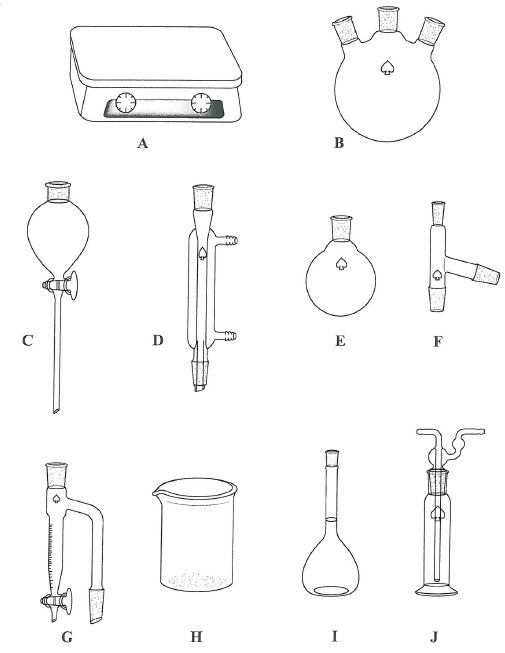
A : balance de prťcision, pesťe d'un solide ou d'un liquide.
B : ballon tricol, synthŤse organique.
C : ampoule ŗ dťcanter, sťparation de deux liquides non miscibles.
D : rťfrigťrant ŗ eau, condensation des vapeurs lors d'une distillation ou d'un chauffage ŗ reflux.
E : ballon col rodť, distillation sous vide.
F : tÍte de distillation utilisť dans une distillation ou une hydrodistillation
G : un tube dťcanteur permet de sťparer l’eau formťe du reste du milieu rťactionnel, par
distillation.
H : becher, mesure peu prťcis d'un volume.
I : fiole jaugťe, mesure prťcis d'un volume.
J : flacon de garde, situť entre la fiole et la trompe ŗ eau, pour empÍcher les retours d'eau vers la fiole ŗ vide.
|
|
