Dosage de l'acide
ascorbique : titrages acido-basique et oxydo-rťduction, Capes 2014.
En poursuivant votre navigation sur ce site, vous acceptez l’utilisation de Cookies vous proposant des publicitťs adaptťes ŗ vos centres d’intťrÍts.
|
|
.
.
|
|
|
|
|
|
|
L'ťtiquette
du mťdicament est reproduite :
Sulfate ferreux :172,73 mg soit fer : 50 mg
acide ascorbique ( vitamine C) : 30 mg
magnťsium carbonate ; talc ; silice ; amidon de maÔs ; enveloppe de la
gelule : gťlatine, titane dioxyde, bleu patentť, jaune de quinolťÔne.
Le professeur dťsire dťterminer la quantitť d'acide ascorbique contenu
dans la gťlule de Timofťrol. Il retient deux mťthodes classiques de
dosage adaptťes ŗ la classe de terminale S : un titrage acide-base et
un titrage d'oxydo-rťduction.
Le
protocole de dissolution d'une gťlule de Timofťrol proposť aux ťlŤves
est le suivant :
Placer le contenu d'une gťlule dans une fiole jaugťe de 100,0 mL.
Ajouter de l'eau distillťe au 3/4 de la fiole et agiter.
Complťter au trait de jauge avec de l'acide sulfurique concentrť.
Titrage
acido-basique.
L'acide ascorbique AscH2 est un acide faible.
Donner la
reprťsentation topologique de sa base conjuguťe en justifiant la rťponse.
L'ion ascorbate est stabilisť par rťsonance.
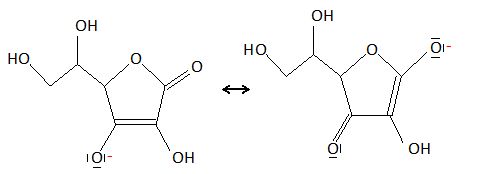
proposer une solution titrante adaptťe. ( Indiquer sa composition et proposer une valeur pour sa concentration, en justifiant succinctement les choix ).
M(C6H8O6) = 6*12+8+6*16 =176 g/mol.
Quantitť de matiŤre d'acide ascorbique contenu dans une gťlule : 0,030 / 176 = 1,7 10-4 mol.
La gťlule est dissoute dans de l'eau distillťe ( fiole jaugťe de 100 mL
). La concentration en acide ascorbique est alors : 1,7 10-4/0,10 = 1,7 10-3 mol/L.
Une solution de soude de concentration 2,0 10-3 mol/L peut convenir : le volume ajoutť ŗ l'ťquivalence sera ( pour une prise de 10 mL d'acide ascorbique ) : Vťq = 10*1,7 10-3 / (2,0 10-3) =8,5 mL.
Cette valeur est assez grande, tout en restant infťrieure ŗ 25 mL, volume de la burette graduťe contenant la soude.
Ecrire l'ťquation de la rťaction de titrage et proposer une mťthode pour dťterminer expťrimentalement le volume ťquivalent.
AscH2aq + HO-aq ---> AscH-aq + H2O(l).
Suivi pHmťtrique ou utiliser un indicateur colorť acido-basique ( BBT).
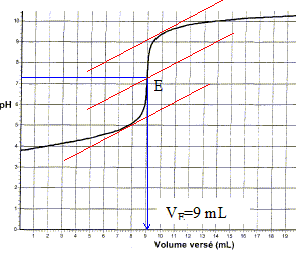
Pourquoi le professeur ne retient-il finalement pas cette mťthode pour doser l'acide ascorbique dans la gťlule ? La dissolution de la gťlule ( principes actifs et excipients) doit Ítre rťaliser en milieu acide sulfurique.
Pratiquer ensuite un dosage acido-basique conduirait ŗ doser l'acide sulfurique ( en large excŤs ) et l'acide ascorbique.
|
|
|
Titrage d'oxydo-rťduction.
La seconde mťthode proposťe est un titrage d'oxydorťduction de l'acide ascorbique AscH2 par une solution d'ions triiodure I3-.
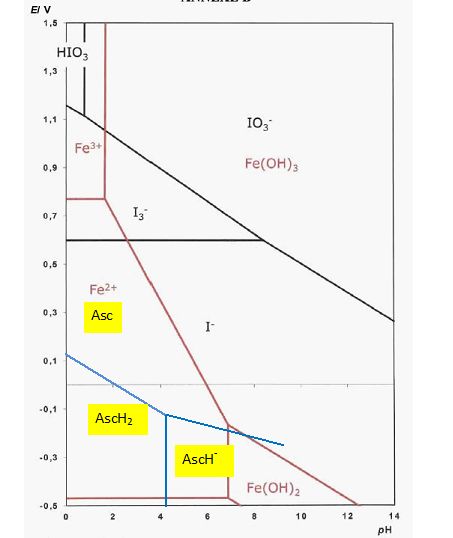
Sur le diagramme fourni, tracer
le diagramme potntiel-pH des espŤces dťrivťes de l'acide ascorbique en
y plaÁant les domaines de prťdominance des espŤces Asc, AscH- et AscH2. ( les concentrations totales en espŤces dissoutes sont 0,10 mol/L).
Eį( Asc / AscH2) = 0,13 V ŗ 25įC ; pKa(AscH2/AscH-) = 4,2.
pH< 4,2.
Asc+2H++2e- = AscH2.
Equation de Nernst : E = 0,13 + 0,03 log [Asc][H+]2 / [AscH2].
E = 0,13 -0,06 pH + log [Asc] / [AscH2]
Equation de la droite frontiŤre : E = 0,13 -0,06 pH.
pH= 4,2.
La droite frontiŤre verticale sťpare les domaines de AscH2 et AscH-.
pH > 4,2.
Asc+H++2e- = AscH-.
Equation de Nernst : E = Eį(Asc/AscH-) + 0,03 log [Asc][H+] / [AscH-].
E = Eį(Asc/AscH-) -0,03 pH + log [Asc] / [AscH-]
Equation de la droite frontiŤre : E = 0,13 -0,03 pH.
|
.
|
|
Justifier la pertinence du choix de la solution titrante et ťcrire l'ťquation de la rťaction du titrage.
La diffťrence des potentiel standard des couples (Asc /AscH2) et ( I3-/I-) est proche de 0,5 V.
Oxydation de l'acide ascorbique, rťducteur le plus fort : AscH2 = Asc + 2H+ + 2e-.
Rťduction de l'ion I3-, oxydant le plus fort : I3- +2e- = 3I-.
Bilan : AscH2 + I3- = Asc + 2H+ +3I-.
Pourquoi ce titrage doit-il Ítre effectuť en milieu acide ?
Il y a dismutation en milieu basique de I3- en ion iodure et en ion IO3- .
|
La prťsence d'ion Fe2+ pose-t-elle problŤme ? Justifier.
Les domaines de prťdominance des ions Fe2+ et I3- ont une partie commune en milieu acide. La prťsence d'ion fer II ne pose pas problŤme.
La
rťalisation pratique de ce titrage conduit ŗ une difficultť : la
texture de la solution de Timofťrol s'ťpaissit lors de l'addition de la
solution titrante et prend une couleur violacťe.
Proposer une explication en consultant l'ťtiquette du Timofťrol.
L'un des excipients est l'amidon de maÔs.
En prťsence d'empois d'amidon, le diiode donne une coloration violet foncťe ŗ la solution.
|
|