|
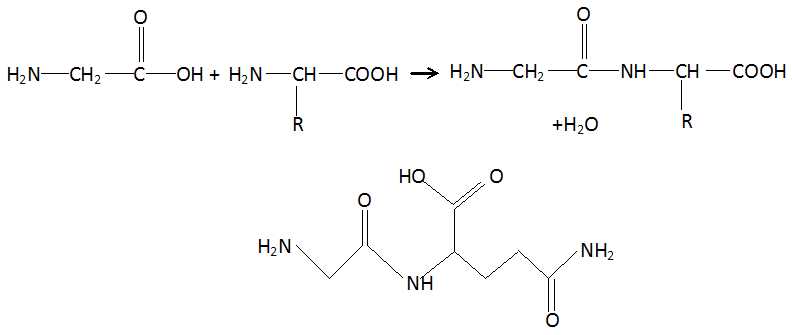
Ecrire
l'équation entre les deux acides a-aminés
dont l'une des deux fonctions est bloquée.
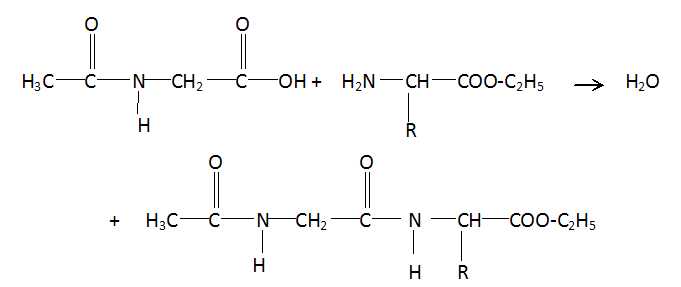
Quelle
réaction peut-on faire pour débloquer les deux fonctions ? Ecrire
l'équation de la réaction qui doit avoir lieu.
Hydrolyse acide dans des conditions douces.
On désire
obtenir 100 g du dipeptide Gly-Gln.
Quelle
masse de glycine et de glutamine faut-il utiliser si le rendement
global de la synthèse est de 65 % ?
M (Gly) =2*12+2*16+14+5 =75 g/mol ; M(Gln) =12*5 +2*14 +3*16 +10 =146
g/mol ; M(gly-Gln) =7*12+3*14+4*16+13=203 g/mol.
n((gly-Gln) =100 / 203 =0,4926 mol ; n(Gly) = n(Gln) = 0,4926 mol.
m(Gly) =0,4926 *75 =36,95 g ; m(Gln) =0,4926*146 =71,9 g.
Tenir compte du rendement : m(Gly) =36,95 / 0,65 ~ 57
g ; m(Gln) =71,9 / 0,65 ~1,1 102
g.
|