.
|
Etude cinétique.
Deux
mélanges eau/acétone sont étudiés à différentes températures. L'eau est
en large excès et intervient comme solvant et comme réactif. Le tableau
suivant résume les conditions opératoires.
|
Eau
|
Acétone
|
2-chloro-2-méthylpropane
|
Température (°C)
|
Expérience A1
|
30 g
|
20 g
|
1,0 mL
|
25
|
| Expérience A2 |
30 g
|
20 g
|
1,0 mL
|
30
|
| Expérience A3 |
30 g
|
20 g
|
1,0 mL
|
40
|
| Expérience B |
25 g
|
25 g
|
1,0 mL
|
40
|
Le
mélange eau/acétone est introduit dans un becher de 100 mL qui est
placé dans un bain thermostaté. Lorsque la température à l'intérieur du
becher est stabilisée à la valeur désirée, une sonde conductimétrique
est introduite puis1,0 mL de 2-chloro-2-méthylpropane est versé dans le
milieu réactionnel sous agitation. Au bout de quelques secondes,
l"'agitation est stoppée puis a conductivité de la solution est suivie
au cours du temps à l'aide d'un système informatisé. La durée de
l'acquisition est de 20 minutes pour chaque étude.
On suppose que s(t) = K x(t) où s(t)
représente la conductivité de la solution à un instant donné diminué de
la conductivité initiale, K est une constante et x(t) représente
l'avancement de la réaction à la date t.
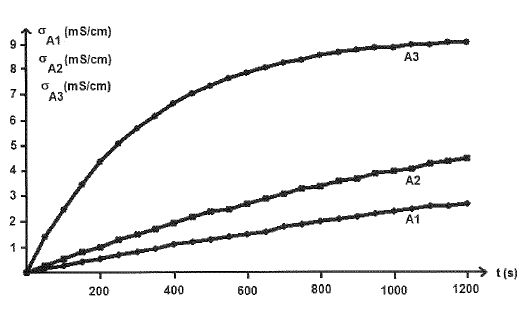
Indiquer l'influence de la température sur la vitesse de la réaction.
A
une date donnée, la conductivité de la solution, donc l'avancement x(t)
sont d'autant plus grands que la température est plus élevée. La
température est un facteur cinétique.
En comparant les expériences A3 et B, indiquer l'influence de la proportion eau/acétone sur la vitesse de la réaction.
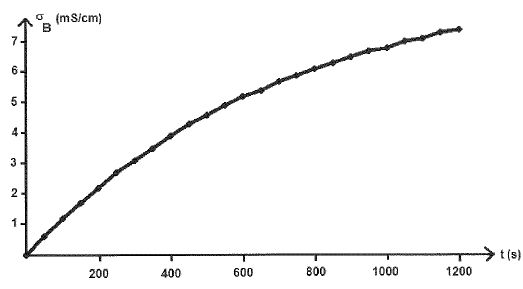
A
une date donnée, à température identique, la conductivité de la
solution, donc l'avancement (x(t), dépendent de la proportion
eau/acétone. Un solvant polaire, l'eau favorise la substitution. En
présence d'une plus grande proportion d'acétone, moins polaire que
l'eau, la vitesse de la réaction décroît.
Définir le temps de demi-réaction et le déterminer dans le cas de l'expérience A3.
Le temps de demi-réaction t½ est la durée au bout de laquelle l'avancement est égal à la moitié de l'avancement final.
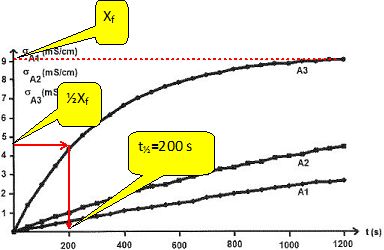
|
Cinétique relativiste.
On
imagine que la réaction est réalisée dans une navette spatiale
s'éloignant à une vitesse v = 0,8 c de la terre où c représente la
célérité de la lumière dans le vide. Les élèves enregistrent un temps
de demi-réaction de 1000 s dans la navette. Un observateur terrestre
peut aussi en déduire une mesure du temps de demi-réaction à l'aide
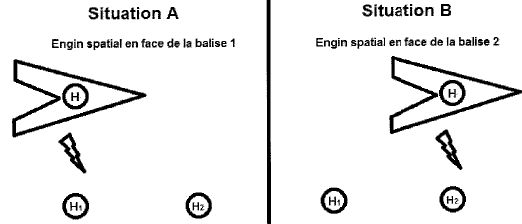
d'un dispositif embarqué dans l'engin qui va envoyer un signal lumineux
à deux balises fixes par rapport à la terre, placées dans l'espace, et
munies de deux horloges H1 et H2 synchronisées.
Un premier signal est envoyé au début de la réaction et un second
lorsque le temps de demi-réaction est atteint. L'horloge H est fixe par
rapport à la navette
Définir la notion de temps propre.
Le temps propre( Dtp)
est la durée séparant deux événements se produisant au même endroit
dans un référentiel galiléen( R). Une horloge fixe dans ce référentiel
(R) mesure le temps propre.
Indiquer les deux référentiels étudiés ici.
Le référentiel terrestre ou un référentiel lié aux deux balises fixes par rapport à la terre et le référentiel de la navette spatiale.
Donner les noms de Dtm et Dtp dans la relation Dtm = g Dtp. Dans quels référentiels sont mesurés ces temps ?
Le temps mesuré ( Dtm)
est la durée séparant deux événements se produisant au même endroit
dans un référentiel galiléen( R') en mouvement par rapport au
référentiel (R). Deux horloges synchronisées, une sur chaque balise fixe détermine le
temps mesuré.
Quel est le nombre suffisant d'horloge(s) qu'il faut pour mesurer le temps propre ?
Une horloge à bord de la navette spatiale mesure le temps propre.
Calculer g. Calculer la durée inconnue.
On donne 1/g2 = 1-v2/c2.
1/g2 =1-0,82 = 0,36 ; g2 =2,78 ; g = 1,67 ~1,7.
Dtm =1,67 *1000 ~1,7 103 s.
Dtm est supérieure à Dtp. Le temps s'écoule plus lentement dans la navette d'après des observateurs terrestres.
Citer une expéreince réaliste qui permet d'observer ce phénomène.
Des particules instables se désintègrent plus lentement du point de vue
de l'observateur lorsqu'elles sont en mouvement à grande vitesse par
rapport à cet observateur.
Le système GPS est tellement précis qu’il est nécessaire d’effectuer des corrections de relativité restreinte.
|
|