|
Concours aide laboratoire Montpellier 2000. |
|||||||
| .
. |
|||||||
|
|||||||
|
Pour
préparer une expérience
de calorimétrie, on souhaite introduire une quantité d'eau d'environ
100 mL
dans un calorimètre de capacité calorifique connue, dont la masse à
vide est
d'environ 250 g. La
masse d'eau doit être
déterminée avec une précision de 0,2 g. On
dispose au laboratoire de
trois types de balances numériques dont les caractéristiques
respectives sont: - portée 300 g précision
0,001 g ; - portée 600 g précision
0,01 g ; - portée 2 000 g précision
0,l g et
de la verrerie suivante : - éprouvette graduée de 250
mL ; - bécher de 250 mL; - fiolejaugée de 250mL ; - pipette de 25 mL. Indiquez clairement
les opérations successives à effectuer et les
appareils les plus appropriés, choisis, en justifiant votre choix. Parmi les 3
résultats
suivants, quel est celui que peut avoir trouvé l'opérateur pour la
masse d'eau
prélevée : 98,2 g ; 100,00
g ; 150,1 g.
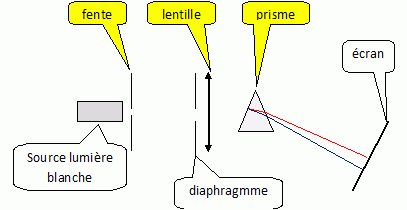
On veut
projeter le spectre
de la lumière blanche sur un écran. Faire un schéma
montrant la
disposition des différents éléments suivants : Pour obtenir le spectre de
la lumière blanche
Vous devez débrancher le cordon
d'alimentation d'un ordinateur en cours de fonctionnement sur une
application
"Windows" : 1. Appuyer sur
"Reset" ; 2. Cliquer
dans le menu de
l'application sur "Fichier" puis "Quitter" 3. Enlever le cordon
d'alimentation de l'unité centrale ; 4. Cliquer
dans le menu de
l'application sur "Fichier" puis "Fermer" 5. Éteindre le moniteur ; 6. Éteindre l'unité centrale ; 7. Cliquer
sur le bouton
"Arrêt" de "Windows" Cliquer dans le menu de
l'application sur "Fichier" puis "Fermer" ;
Vous observez sur l'écran
d'un oscilloscope à deux voies (A et B) la trace d'un signal sinusoïdal
de
fréquence 100 Hz, branché sur la voie A, mais cette trace défile
lentement vers
la gauche et vous voulez la stabiliser. Quels sont les
réglages
susceptibles de remédier au défilement : 1. Changer la voie de
déclenchement ; 2. Agir sur la base de
temps ; 3. Agir
sur le niveau de
déclenchement 4. Agir
sur la sensibilité
verticale de la voie B ; Se placer en
déclenchement automatique. Donnez la formule chimique des produits suivants : Soude : NaOH ; acide chlorhydrique HCl ; acide sulfurique H2SO4 ; potasse
KOH ; acide
nitrique HNO3.
Associez une formule
à un
nom dans les listes suivantes : Fe2(SO4)3
sulfate de fer III
; C2H4 éthylène ; H2C = 0
méthanal ; NH3 ammoniac.
On veut préparer une
solution titrée à partir d'une solution mère d'hydroxyde de sodium. Pour cela on doit prélever 20,0 mL à partir
d'un flacon de 1 litre de solution mère. Choisir dans la
liste
suivante, les opérations les plus appropriées :
|
|||||||
| |
|||||||
|
|