|
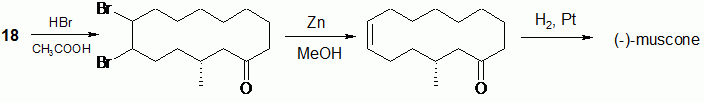
Synthèse de la muscone, concours inspecteur répression des fraudes 2009. |
|||||||
| .
. |
|||||||
|
|||||||
|
Le
cerf musqué possède, près de
l'estomac, une glande produisant des substances à odeur musquée. L'une
de ces
substances, la muscone, a été isolée pure par Walbaum en 1906 et sa
structure a
été déterminée par Ruzicka en 1926. Il existe plusieurs synthèses
conduisant à
la formation de la muscone : nous allons nous intéresser à celle
proposée par
Mamdapur et son équipe en 1926. Elle présente en effet l'intérêt de
prendre
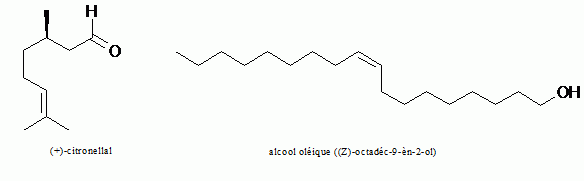
comme réactifs de départs deux composés naturels :
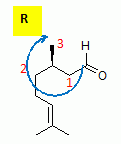
Que
signifie le (+) ? Le (+) citronellal possède un atome de carbone asymétrique : il est donc chiral. CH2 -CHO (1) ; CH2-CH2-CH=C(CH3)2
(2) ; CH3 (3) ; H (4).
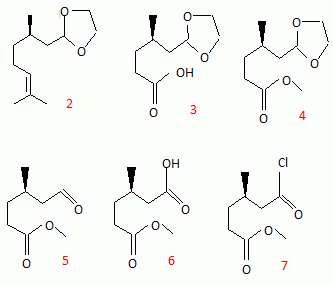
Ce
composé est traité par le glycol
(éthane-1,2-diol) en milieu anhydre en présence d'APTS (Acide
ParaToluèneSulfonique), on obtient le composé 2. Le
composé 2 est
alors soumis à une ozonolyse suivie d'une hydrolyse en milieu oxydant.
On
obtient de l'acétone et le composé 3.
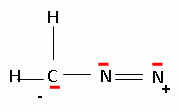
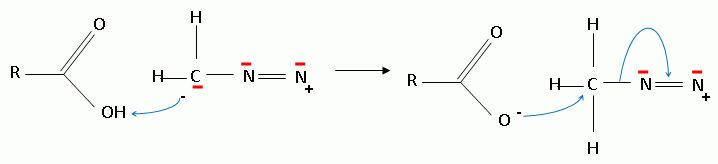
Ce produit est estérifié par le diazométhane pour donner 4.
4 subit une hydrolyse
acide pour former 5 qui est alors
oxydé en 6. Le traitement de 6 par le
chlorure de thionyle SOCl2
conduit à 7. Donner les structure des composés 2 à 7.
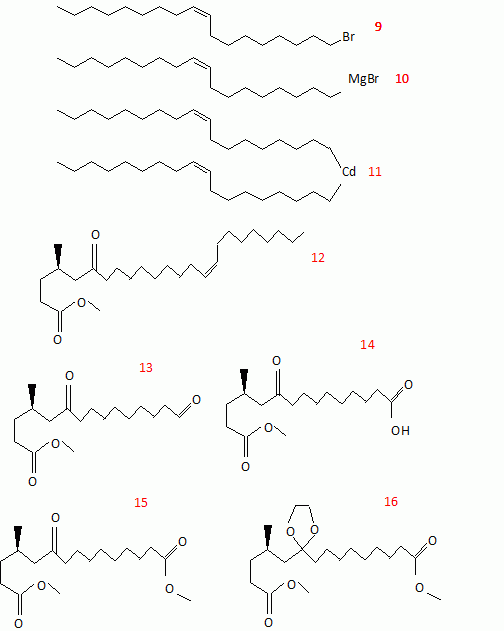
L'alcool oléique est traité par le tribromure de phosphore et le composé 9 obtenu est soumis à l'action du
magnésium dans l'éther anhydre pour former 10.
Le traitement de 10 par du chlorure
de cadmium donne 11 qui réagit avec 7 pour former 12 de formule brute C26H48O3. 12 subit une ozonolyse suivi d'une
hydrolyse en milieu réducteur pour former le composé 13 qui contient 17 atomes de carbone. L'oxydation chromique de 13 conduit à 14 qui est estérifié en 15
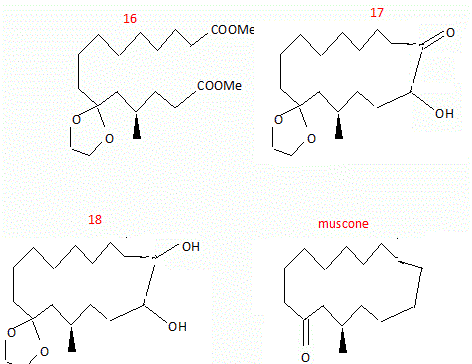
par le méthanol. L'action du glycol en milieu acide anhydre conduit à la
formation de 16. Quel est l'intérêt du passage 10 à 11 ? Le remplacement de l'organomagnésien par un organocadmien permet de s'arrêter au stade cétone. Les cétones moins réactives que les chlorures d'acyles ne réagissent pas avec les organocadmiens.
|
|||||||
| |
|||||||
|
|