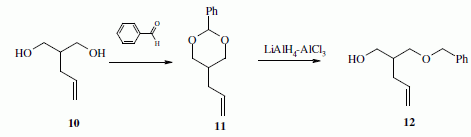|
chimie organique : RMN, ťnantiomŤres, diastťrťoisomŤres, acťtal, concours chimie agrťgation 2008. En poursuivant votre navigation sur ce site, vous acceptez l’utilisation de Cookies vous proposant des publicitťs adaptťes ŗ vos centres d’intťrÍts. |
|||||||||||||||||||||||||||||||||||||||
| .
. |
|||||||||||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||||||||||
|
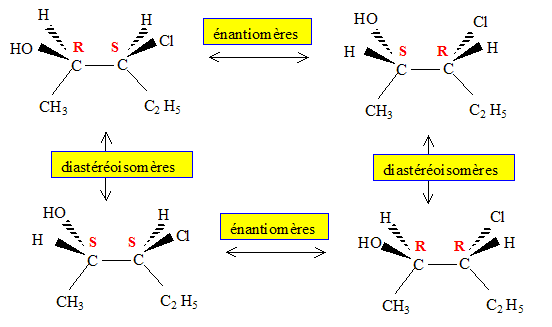
Dťfinir chiralitť, ťnantiomťrie, diastťrťoisomťrie. Chiralitť : dťsigne la propriťtť d'un objet de ne pas Ítre superposable ŗ son image dans un miroir ( ou dans une symťtrie par rapport ŗ un plan). Une main n'est pas superposable ŗ son image dans un miroir. Une molťcule comptant un atome de carbone asymťtrique est chirale Deux ťnantiomŤres ne diffťrent que par leur propriťtťs optiques ; ils sont sťparables. Ce sont 2 isomŤres de configuration, images l'un de l'autre dans un miroir. ę diastťrťoisomŤres Ľ : encore stťrťoisomŤres qui ne sont pas des ťnantiomŤres. Des isomťres cis- et trans- (ou Z et E) sont des diastťrťoisomŤres.
Illustration expťrimentale mettant en ťvidence les propriťtťs diffťrentes de deux ťnantiomŤres. - Cas de la deltamťthrine :l'un des ťnantiomŤre a des propriťtťs insecticides, l'autre n'en possŤde pas. - Les deux ťnantiomŤres du citronellal donnent les arŰmes de citron et d'orange. Le non dťdoublement d'ťnantiomŤres dans un mťdicament a eu des consťquences dramatiques dans les annťes 1960 : les deux ťnantiomŤres de la molťcule active ont un effet sťdatif, mais l'ťnantiomŤre (S) a en plus un effet tťratogŤne. Rappeler le nom de ce mťdicament et la signification du mot tťratogŤne. La thalidomide ; issu du grec, le terme tťratogŤne signifie ę crťation de monstres Ľ. Le mot "racťmique" vient du latin racemus qui signifie grappe de raisin. Le premier dťdoublement d'un mťlange racťmique a ťtť rťalisť par Pasteur. Comment a t-il rťalisť cette sťparation ? Quel est le rapport avec la grappe de raisin ? Situer l'ťpoque de cette sťparation. Vers 1860, Pasteur sťpare manuellement avec une petite pince
des cristaux d'acide tartrique ťnantiomŤres. L'acide tartrique ťtait
issu du jus de raisin. La monensine possŤde des propriťtťs antibiotiques
intťressantes pour lutter contre les infections coccidiennes ( maladies
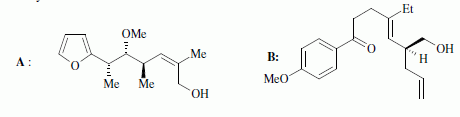
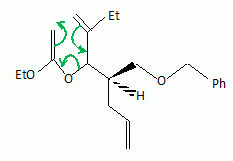
du bťtail ). Nous ťtidions ici partiellement la synthŤse de deux
fragments A et B nťcessaires ŗ la synthŤse totale de la
monensine, qui fut rťalisťe en 1979 par Y Kishi.
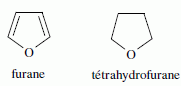
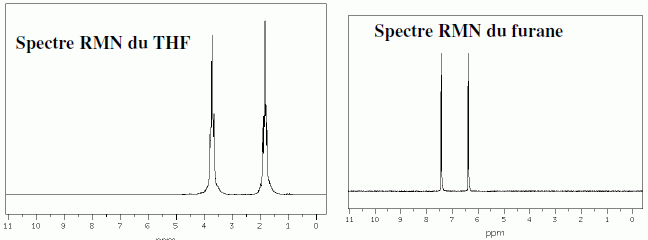
Pour le furane, comme pour le THF, les protons les plus dťblindťs sont situťs en position a de l'atome d'oxygŤne. Deux isomŤres I1 et I2 du THF ont des spectres caractťrisťs par les signaux ci-dessous. 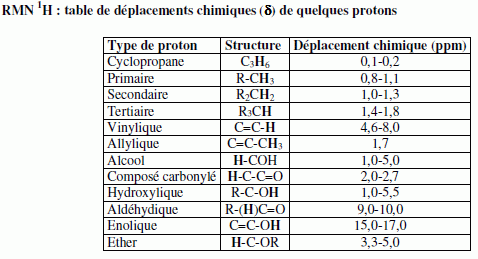 Identifier I1 et I2.
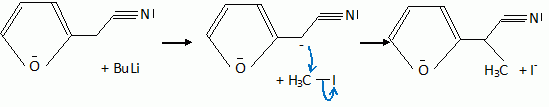
Quelques aspects de la synthŤse de A. Le 2-furilacťtonitrile 1 est traitť par du butyllithium ( Buli) dans le tťtrahydrofurane ( THF), puis est opposť ŗ l'iodure de mťthyle MeI : on obtient le composť 2. Celui-ci est ensuite chauffť ŗ reflux dans un solvant mťthanol-eau pour obtenir le produit 3. 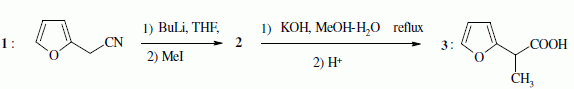 Le composť 1 possŤde un hydrogŤne lťgŤrement acide : justifier en ťcrivant les formes mťsomŤres de la base conjuguťe. 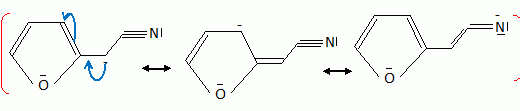 Proposer un schťma rťactionnel pour
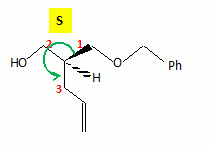
le passage de 1 ŗ 2. Hydrolyse de la fonction nitrile -CN en acide carboxylique. Le composť 3 possŤde un atome de carbone asymťtrique : obtient-on les deux ťnantiomŤres ? Justifier. Dans l'ťtape 1-->2, le carbanion ne possŤde pas une configuration particuliŤre : la rťaction 1 --> 2 n'est pas stťrťosťlective : le mťlange racťmique est donc obtenu. La suite de la synthŤse est rťalisťe avec un seul des deux ťnantiomŤres, 3' : 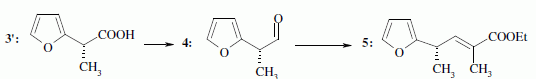 Donner la configuration absolue de l'atome de carbone asymťtrique de 3' en justifiant. Numťroter de faÁon dťcroissante chacun des quatre substituants selon son numťro atomique. (1) -COOH ; (2) cycle ; (3) CH3 ; (4) H. On place alors l'atome (ou le groupement) de numťro le plus ťlevť derriŤre. On regarde dans quel sens, sens horaire ou trigonomťtrique, on passe du numťro 1, au 2, au 3. - Si le sens de rotation est le sens horaire (ou anti-trigonomťtrique), le carbone est Rectus (R), - Si le sens de rotation est le sens trigonomťtrique (ou anti-horaire), le carbone est Sinister (S). 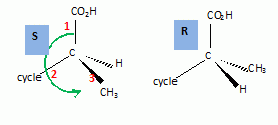 L'atome de carbone asymťtrique
est donc R. L'atome de carbone asymťtrique
est donc R.Le passage de 4 ŗ 5 est une rťaction de Wittig : quel est le rťactif utilisť pour rťaliser cette transformation ? Les ylures de phosphore sont p dans la rťaction de Wittig : ils rťagissent sur des carbonyles ( aldehyde ou cťtone ) pour conduire ŗ des dťrivťs ťthylŤniques. 
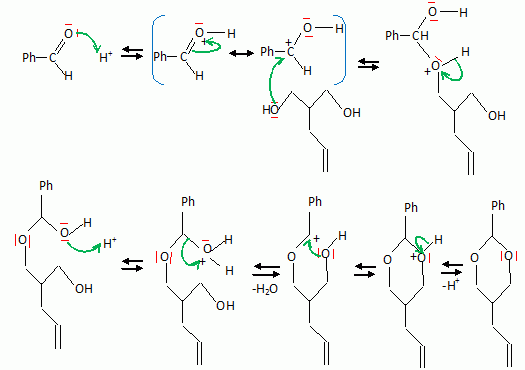
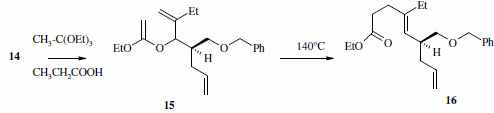
La suite de la synthŤse se dťroule comme suit :
|
|||||||||||||||||||||||||||||||||||||||
| |
|||||||||||||||||||||||||||||||||||||||
|
|